题目内容
2mol H2和2mol CO2相比较,下列叙述正确的是( )
| A、分子数相等 | B、原子数相等 |
| C、体积相等 | D、质量相等 |
考点:物质的量的相关计算
专题:计算题
分析:A、根据n=
分析;
B、由分子组成分析原子数;
C、气体的摩尔体积可能不同;
D、二者的摩尔质量不相等.
| N |
| NA |
B、由分子组成分析原子数;
C、气体的摩尔体积可能不同;
D、二者的摩尔质量不相等.
解答:
解:A、2mol H2和2mol CO2均有2NA个分子,故A正确;
B、2mol H2和2mol CO2分子数相同,原子数之比为2:3,故B错误;
C、气体的摩尔体积可能不同,因此2mol H2和2mol CO2的体积不一定相同,故C错误;
D、H2和 CO2的物质的量相等,但摩尔质量不相等,因此质量不等,故D错误;
故选A.
B、2mol H2和2mol CO2分子数相同,原子数之比为2:3,故B错误;
C、气体的摩尔体积可能不同,因此2mol H2和2mol CO2的体积不一定相同,故C错误;
D、H2和 CO2的物质的量相等,但摩尔质量不相等,因此质量不等,故D错误;
故选A.
点评:本题考查物质的量的有关计算,注意理解有关公式及阿伏伽德罗定律的推论,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
检验氯化氢气体中是否混有氯气,可采用的方法是( )
| A、用干燥的蓝色石蕊试纸 |
| B、用湿润的有色布条 |
| C、将气体通入硝酸银溶液 |
| D、将气体通入氢氧化钠溶液 |
“绿色奥运”是2008北京奥运会的主题之一.为减轻污染,北京为汽车加装了“三效催化净化器”,可将尾气中的一氧化碳、一氧化氮转化为参与大气循环的无毒混合气体,该气体是( )
| A、二氧化碳和氮气 |
| B、二氧化碳和二氧化氮 |
| C、二氧化碳和氧气 |
| D、二氧化碳和氧化二氮 |
下列各组物质不加其它试剂不能鉴别的是( )
| A、盐酸、氢氧化钠溶液、石蕊试液 |
| B、盐酸、氢氧化钠溶液、酚酞 |
| C、氢氧化钠溶液、氢氧化钡溶液、硫酸 |
| D、硫酸铜溶液、盐酸、氢氧化钠溶液 |
一包混有杂质的Na2CO3,其杂质只可能是Ba(NO3)2、KCl、NaHCO3、K2CO3中的一种或几种,今取10.6g样品,溶于水得澄清溶液,另取10.6克样品,加入足量的盐酸,收集到4.4gCO2,则下列判断正确的是( )
| A、样品中只混有NaHCO3 |
| B、样品中一定混有NaHCO3,可能混有KCl,也可能混有K2CO3 |
| C、样品中混有NaHCO3,也混有Ba(NO3)2 |
| D、样品中混有KCl,也可能混有NaHCO3 |
阿伏加德罗常数约为6.02×1023mol-1,用NA表示,下列说法中一定正确的是( )
| A、100mL 2.0mol/L的盐酸溶液中氢离子数为2NA |
| B、0.1mol CH4所含的电子数为1NA |
| C、Na2O2与H2O反应生成1.12LO2(标准状况),反应中转移的电子数为2×6.02×1022 |
| D、标准状况下,22.4L Cl2和HCl的混合气体中含分子总数为2×6.02×1023 |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
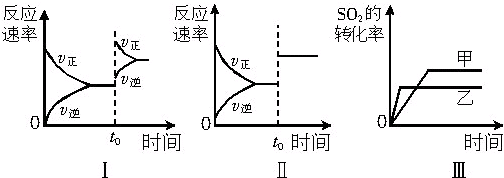

| A、图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 |
| B、图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |