题目内容
7.把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上没有(填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来,组成一个原电池,正极的电极反应式为2H++2e-═H2↑.分析 铜不活泼,与硫酸不反应,锌和铜形成原电池时,锌为负极,铜为正极,正极上生成氢气,由此分析解答.
解答 解:铜片插入稀硫酸中时,二者不反应,没有气泡产生,但当把铜片和锌片用导线相连插入稀硫酸中时,会构成原电池,铜作为原电池正极,电极反应为2H++2e-═H2↑,锌作为原电池负极,电极反应为Zn-2e-═Zn2+,电池总反应为Zn+2H+═Zn2++H2↑,故答案为:没有;2H++2e-═H2↑.
点评 本题考查原电池知识,侧重于学生的基础知识的综合运用,注意把握原电池的工作原理,学习中注意体会,难度不大.

练习册系列答案
相关题目
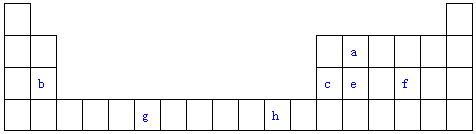
18.A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表:
请回答下列问题(用对应元素的元素符号作答):
(1)写出D元素基态原子的价电子排布式3s23p1,E2+价电子的轨道表示式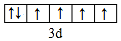 .
.
(2)这5种元素中电负性最大的元素是O(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为N>O>C(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为N3->O2->Al3+(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式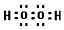 .
.
| 元素 | 相关信息 |
| A | 基态原子的价电子排布式为nSnnPn |
| B | 基态原子中的未成对电子数是同周期中最多的 |
| C | 最外层电子数是电子层数的3倍 |
| D | 简单离子是第三周期元素中离子半径最小的 |
| E | 价电子层中的未成对电子数为4 |
(1)写出D元素基态原子的价电子排布式3s23p1,E2+价电子的轨道表示式
 .
.(2)这5种元素中电负性最大的元素是O(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为N>O>C(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为N3->O2->Al3+(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式
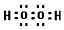 .
.
15. 如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
 如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )| A. | 电流表指针不发生偏转 | |
| B. | Al、Pt两极有H2产生 | |
| C. | 甲池pH增大,乙池pH减小 | |
| D. | Mg、C两极生成的气体在一定条件下可以恰好完全反应 |
2.下列说法正确的是( )
| A. | 水溶液中能电离出H+的化合物叫做酸 | |
| B. | 实验测得2mol某气体体积为44.8L,则测定条件一定是标准状况 | |
| C. | 摩尔是七个基本物理量之一 | |
| D. | 化合物分为酸、碱、盐和氧化物是用树状分类法分类的 |
12.往浅绿色的Fe(NO3)2溶液中逐滴加入稀盐酸时,溶液的颜色变化应该( )
| A. | 颜色变浅 | B. | 逐渐变红色 | C. | 没有改变 | D. | 变棕黄色 |
19.烯烃、炔烃因含不饱和键能被酸性KMnO4溶液氧化,下列各物质中不属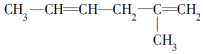 被酸性高锰酸钾氧化的产物的是( )
被酸性高锰酸钾氧化的产物的是( )
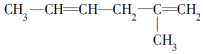 被酸性高锰酸钾氧化的产物的是( )
被酸性高锰酸钾氧化的产物的是( )| A. | CO2 | B. | CH3COOH | ||
| C. | 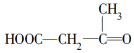 | D. | HOOC-CH2-CH2-COOH |
17.煤的液化可以合成甲醇.下列有关说法正确的是
①“气化”:C(s)+2H2O(g)═CO2(g)+2H2(g);△H1=90.1kJ•mol-1
②催化液化I:CO2(g)+3H2(g)═CH3OH(g)+H2O(g);△H2=-49.0kJ•mol-1
③催化液化 II:CO2(g)+2H2(g)═CH3OH(g)+$\frac{1}{2}$O2(g);△H3=akJ•mol-1( )
①“气化”:C(s)+2H2O(g)═CO2(g)+2H2(g);△H1=90.1kJ•mol-1
②催化液化I:CO2(g)+3H2(g)═CH3OH(g)+H2O(g);△H2=-49.0kJ•mol-1
③催化液化 II:CO2(g)+2H2(g)═CH3OH(g)+$\frac{1}{2}$O2(g);△H3=akJ•mol-1( )

| A. | 催化液化I中使用催化剂,反应的活化能Ea、△H2都减小 | |
| B. | 反应C(s)+H2O(g)+H2(g)=CH3OH(g)△H=41.1 kJ•mol-1 | |
| C. | △H2>△H3 | |
| D. | 图为甲醇燃料电池的工作原理,负极的电极反应为:CH3OH-6e-+6OH-═CO2+5H2O |