题目内容
 将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图,则下列说法正确的是( )| A、整个过程中阳极先产生Cl2,后产生O2 |
| B、阳极极产物一定是Cl2,阴极产物一定是Cu |
| C、BC段表示在阴极上是H+放电产生了H2 |
| D、CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+ |
考点:电解原理
专题:
分析:设CuSO4的和NaCl各nmol,电解分3个阶段:AB段:阳极:nmol氯离子失nmol电子,阴极:
nmol铜离子得nmol电子,由于铜离子水解使溶液酸性减弱,铜离子浓度逐渐减小,溶液pH值逐渐增大;BC段:阳极:nmol氢氧根离子失nmol电子(来源于水的电离),阴极:
n mol铜离子再得nmol电子,由于氢氧根离子消耗,溶液中氢离子浓度增大,溶液的pH值迅速减小;CD段:阳极:氢氧根离子失去电子,阴极:氢离子得到电子,开始电解水,溶液中氢离子浓度逐渐增大,pH值减小,
根据以上分析进行判断.
| 1 |
| 2 |
| 1 |
| 2 |
根据以上分析进行判断.
解答:
解:设CuSO4的和NaCl各nmol,电解分3个阶段:
AB段:阳极:nmol氯离子失nmol电子,阴极:
nmol铜离子得nmol电子,由于铜离子水解使溶液酸性减弱,铜离子浓度逐渐减小,溶液pH值逐渐增大;
BC段:阳极:nmol氢氧根离子失nmol电子(来源于水的电离),阴极:
n mol铜离子再得nmol电子,由于氢氧根离子消耗,溶液中氢离子浓度增大,溶液的pH值迅速减小;
CD段:阳极:氢氧根离子失去电子,阴极:氢离子得到电子,开始电解水,溶液中氢离子浓度逐渐增大,pH值减小,
A、阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑,故A正确;
B、电解开始时,阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑,阴极反应先发生Cu2++2e-═Cu,后发生2H++2e-═H2↑,故B错误;
C、阴极:
n mol铜离子再得nmol电子,由于氢氧根离子消耗,溶液中氢离子浓度增大,溶液的pH值迅速减小,故C错误;
D、CD段发生2H++2e-═H2↑、4OH--4e-═2H2O+O2↑,即CD段电解的物质是水,未产生氢离子,故D错误;
故选:A.
AB段:阳极:nmol氯离子失nmol电子,阴极:
| 1 |
| 2 |
BC段:阳极:nmol氢氧根离子失nmol电子(来源于水的电离),阴极:
| 1 |
| 2 |
CD段:阳极:氢氧根离子失去电子,阴极:氢离子得到电子,开始电解水,溶液中氢离子浓度逐渐增大,pH值减小,
A、阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑,故A正确;
B、电解开始时,阳极先发生2Cl--2e-═Cl2↑,后发生4OH--4e-═2H2O+O2↑,阴极反应先发生Cu2++2e-═Cu,后发生2H++2e-═H2↑,故B错误;
C、阴极:
| 1 |
| 2 |
D、CD段发生2H++2e-═H2↑、4OH--4e-═2H2O+O2↑,即CD段电解的物质是水,未产生氢离子,故D错误;
故选:A.
点评:本题考查电解原理,明确电解过程中离子的移动及离子的放电顺序、发生的电极反应是解答本题的关键,并注意结合图象来分析解答,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、氯气溶于水:Cl2+H2O?2H++Cl-+ClO- |
| C、硫酸溶液中加入铁粉:2Fe+6H+=2Fe3++3H2O |
| D、碳酸氢钠溶液中加入氢氧化钠溶液:HCO3-+OH-=CO32-+H2O |
下列有关化学用语表示正确的是( )
A、CH4分子的球棍模型: | ||
B、Cl-离子的结构示意图: | ||
C、氟化钠的电子式: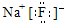 | ||
D、中子数为146、质子数为92 的铀原子
|
关于蛋白质的叙述错误的是( )
| A、在世界上我国首先合成了具有生命活力的蛋白质--结晶牛胰岛素 |
| B、蛋白质是组成细胞的基础物质,它是小分子物质 |
| C、蛋白质水解的最终产物是氨基酸 |
| D、高温灭菌的原理是加热后使蛋白质变性,从而使细菌死亡 |
 全球气候变暖已经成为全世界人类面临的重大问题,温家宝总理在“哥本哈根会议”上承诺到2020年中国减排温室气体40%.
全球气候变暖已经成为全世界人类面临的重大问题,温家宝总理在“哥本哈根会议”上承诺到2020年中国减排温室气体40%.