题目内容
现有下列浓度均为0.1mol/L的电解质溶液:
①Na2CO3、②NaHCO3、③ 、④CH3COONH4、⑤NH4HCO3
、④CH3COONH4、⑤NH4HCO3
(1)上述5种物质的溶液既能与盐酸又能与烧碱溶液反应的是(填写序号) .
(2)已知溶液④呈中性,该溶液中离子浓度由大到小的顺序是 .
(3)已知溶液⑤呈碱性,比较④、⑤两溶液的酸碱性,可以得出的结论是 .
①Na2CO3、②NaHCO3、③
 、④CH3COONH4、⑤NH4HCO3
、④CH3COONH4、⑤NH4HCO3(1)上述5种物质的溶液既能与盐酸又能与烧碱溶液反应的是(填写序号)
(2)已知溶液④呈中性,该溶液中离子浓度由大到小的顺序是
(3)已知溶液⑤呈碱性,比较④、⑤两溶液的酸碱性,可以得出的结论是
考点:钠的重要化合物,铵盐
专题:氮族元素,几种重要的金属及其化合物
分析:(1)既能与盐酸又能与烧碱溶液反应的有两性氧化物、两性氢氧化物、弱酸的酸式盐、弱酸弱碱盐等;
(2)根据④呈中性结合电荷守恒判断;
(3)已知溶液⑤呈碱性,④呈中性,说明醋酸酸性比碳酸强.
(2)根据④呈中性结合电荷守恒判断;
(3)已知溶液⑤呈碱性,④呈中性,说明醋酸酸性比碳酸强.
解答:
解:(1)HCO3-既不与酸共存,也不与碱共存;NH4+不与碱共存,CH3COONH4为弱酸弱碱盐,故既能与盐酸反应,又能与烧碱反应的电解质有②④⑤,
故答案为:②④⑤;
(2))④呈中性c(H+)=c(OH-),又电荷守恒为c(H+)+c(NH4+)=c(CH3COO-)+c(OH-),所以离子浓度由大到小的顺序c(CH3COO-)=c(NH4+)>c(H+)=c(OH-),故答案为c(CH3COO-)=c(NH4+)>c(H+)=c(OH-);
(3)④呈中性,CH3COONH4是弱酸弱碱盐,溶液呈中性,说明CH3COO-和NH4+水解程度相同,但H2CO3酸性弱于CH3COOH,HCO3-的水解程度大于CH3COO-,所以NH4HCO3溶液pH>7,
故答案为:HCO3-的水解程度比CH3COO-大或CH3COOH酸性比H2CO3强.
故答案为:②④⑤;
(2))④呈中性c(H+)=c(OH-),又电荷守恒为c(H+)+c(NH4+)=c(CH3COO-)+c(OH-),所以离子浓度由大到小的顺序c(CH3COO-)=c(NH4+)>c(H+)=c(OH-),故答案为c(CH3COO-)=c(NH4+)>c(H+)=c(OH-);
(3)④呈中性,CH3COONH4是弱酸弱碱盐,溶液呈中性,说明CH3COO-和NH4+水解程度相同,但H2CO3酸性弱于CH3COOH,HCO3-的水解程度大于CH3COO-,所以NH4HCO3溶液pH>7,
故答案为:HCO3-的水解程度比CH3COO-大或CH3COOH酸性比H2CO3强.
点评:本题考查电解质、盐类水解,综合考查学生化学知识的应用能力和分析问题的能力,为高考常见题型,题目难度不大,注意把握盐类水解和弱电解质的电离特点.

练习册系列答案
相关题目
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A、分液、蒸馏、萃取 |
| B、萃取、蒸馏、分液 |
| C、分液、萃取、蒸馏 |
| D、蒸馏、萃取、分液 |
球墨铸铁中含有一种铁碳化合物X.实验室测定化合物X的组成实验如下:下列说法不正确的是( )


| A、固体2是氧化铁 |
| B、X的化学式可以表示为Fe3C2 |
| C、溶液甲中可能含有Fe3+ |
| D、X与足量的热浓硝酸反应有NO2和CO2生成 |
下列关于氧化纳和过氧化钠的叙述中,正确的是( )
| A、都属于碱性氧化物 |
| B、都能与水发生化合反应 |
| C、水溶液的成分相同 |
| D、与二氧化碳反应生成不同的盐 |
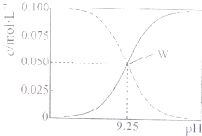 25℃时,将氨水与氯化铵溶液混合得到c(NH3?H2O)+c(NH4+)=0.1mol?L-1的混合溶液.溶液中c(NH3?H2O)、c(NH4+)与pH的关系如图所示.下列有关离子浓度关系叙述一定正确的是( )
25℃时,将氨水与氯化铵溶液混合得到c(NH3?H2O)+c(NH4+)=0.1mol?L-1的混合溶液.溶液中c(NH3?H2O)、c(NH4+)与pH的关系如图所示.下列有关离子浓度关系叙述一定正确的是( )| A、W点表示溶液中:c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
| B、pH=10.5溶液中c(Cl-)+c(OH-)+c(NH3?H2O)<0.1 mol?L-1 |
| C、pH=9.5溶液中c(NH3?H2O)>c(NH4+)>c(OH-)>c(H+) |
| D、向W点所表示1L溶液中加入0.05molNaOH固体(溶液体积变化可忽略):c(Cl-)>c(Na+)>c(OH-)>c(NH4+)>c(H+) |
将浓度为0.1mol/L的HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A、c(H+) |
| B、Ka(HF) |
| C、c(F-) |
| D、c(OH-) |