题目内容
8.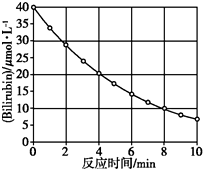 化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )| A. | 2.5 μmol/( L•min)和2.0 μmol/L | B. | 2.5 μmol/( L•min)和2.5 μmol/L | ||
| C. | 3.0 μmol/( L•min)和3.0 μmol/L | D. | 5.0 μmol/( L•min)和3.0 μmol/L |
分析 根据v=$\frac{△c}{△t}$计算反应4~8min间的平均反应速率;0~4 min期间,反应物浓度变化为(40-20)μmol/L=20μmol/L,4~8 min期间,反应物浓度变化为(20-10)μ mol/L=10μmol/L,可知,每隔4分钟,速率降为原来的一半,据此计算.
解答 解:由图可知,4~8 min期间,反应物浓度变化为(20-10)μ mol/L=10μmol/L,
所以4~8 min期间,反应速率为$\frac{10μmol/L}{4min}$=2.5μ mol/(L•min);
由图可知,0~4 min期间,反应物浓度变化为(40-20)μmol/L=20μmol/L,4~8 min期间,反应物浓度变化为(20-10)μ mol/L=10μmol/L,可知,每隔4分钟,浓度变化量降为原来的一半,所以8~12min浓度变化为5μ mol/L,12~16min浓度变化为2.5μ mol/L,
所以16min时浓度为10μ mol/L-5μ mol/L-2.5μ mol/L=2.5μ mol/L.
故选B.
点评 本题考查反应速率的有关计算,难度中等,根据图中浓度变化判断相同时间内的浓度变化量是解题关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.CO2是一种温室气体.CO2属于( )
| A. | 酸 | B. | 碱 | C. | 有机物 | D. | 酸性氧化物 |
10.国际组织无机化学命名委员会将长式周期表原先的主副族族号取消,由左向右按原结构编为18列,如碱金属为第1列,稀有气体为第18列.按这个规定,下列说法不正确的是( )
| A. | 只有第2列元素的原子最外层有2个电子 | |
| B. | 第14列元素形成化合物种类最多 | |
| C. | 第3列元素种类最多 | |
| D. | 第17、18列元素都是非金属元素 |
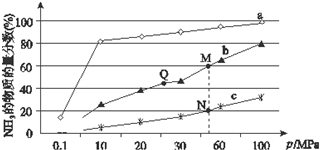 合成氨反应是化学上最重要的反应之一:
合成氨反应是化学上最重要的反应之一: