题目内容
4.下列各组原子中,彼此化学性质一定相似的是( )| A. | 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 | |
| B. | 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 | |
| C. | 2p轨道上有一个空轨道的X原子与3p轨道上有一个空轨道的Y原子 | |
| D. | 最外层都只有一个电子的X、Y原子 |
分析 A.原子核外电子排布式为1s2为He,原子核外电子排布式为1s22s2为Be;
B.原子核外M层上仅有两个电子的X为Mg元素,原子核外N层上仅有两个电子的Y可能为Ca、Sc、Ti、V、Fe、Co、Ni、Zn等元素;
C.2p轨道上只有一个电子的X为B元素,3p轨道上只有一个电子的Y为Al;
D.最外层都只有一个电子的X、Y原子,可能为H与碱金属元素.
解答 解:A.原子核外电子排布式为1s2为He,原子核外电子排布式为1s22s2为Be,二者性质不同,故A错误;
B.原子核外M层上仅有两个电子的X为Mg元素,原子核外N层上仅有两个电子的Y可能为Ca、Sc、Ti、V、Fe、Co、Ni、Zn等元素,但价电子数不同,性质不相同,故B错误;
C.2p轨道上有一个空轨道的X为C元素,3p轨道上有一个空轨道的Y为Si,二者位于周期表同一主族,最外层电子数相同,性质相似,故C正确;
D.最外层都只有一个电子的X、Y原子,可能为H与碱金属元素,性质有相似地方,都具有还原性,但与ⅠB族元素性质不同,虽然最外层也有1个电子,故D错误;
故选C.
点评 本题考查原子的结构和元素的性质,为高频考点,侧重考查学生的分析能力,题目难度不大,注意原子核外电子排布特点与对应元素化合物的性质的关系.

练习册系列答案
相关题目
16.下列说法正确的是(NA为阿伏加德罗常数的值)( )
| A. | 14g氮气含有的原子数为0.5NA | |
| B. | 4 g金属钙变成钙离子时失去的电子数为0.1NA | |
| C. | 1 mol O2分子的质量等于1 mol氧原子的质量 | |
| D. | 16 g O2分子和16g O3分子所含的氧原子数目相等 |
13.在碳酸钙中加入适量盐酸至二者恰好完全反应,得到溶液M.下列离子在溶液M中能大量共存,且所得溶液为无色的是( )
| A. | Na+、K+、Cl-、NO3- | B. | Cu2+、K+、SO42-、NO3- | ||
| C. | Na+、Ag+、NO3-、HCO3- | D. | Na+、NH4+、CO32-、OH- |
14.下列关于同温同压下的两种气体 12C18O和14N2的判断不正确的是( )
| A. | 体积相等时密度不相等 | B. | 原子数相等时具有的中子数不相等 | ||
| C. | 体积相等时具有的电子数相等 | D. | 质量相等时具有的质子数相等 |
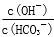 增大
增大
 .
.