题目内容
3. 在某溶液中滴加氢氧化钠溶液产生沉淀的物质的量(n)与氢氧化钠溶液体积(V)的关系如图所示.该溶液中可能含有的离子组是( )
在某溶液中滴加氢氧化钠溶液产生沉淀的物质的量(n)与氢氧化钠溶液体积(V)的关系如图所示.该溶液中可能含有的离子组是( )| A. | Na+、Mg2+、Al3+、NO3-、Cl- | B. | Cu2+、H+、Fe3+、Mg2+、SO42- | ||
| C. | NH4+、H+、Al3+、HCO3-、NO3- | D. | NH4+、H+、Al3+、SO42-、Br- |
分析 由图可知,开始不生成沉淀,则溶液中一定含H+,然后生成沉淀,一段时间沉淀的量不变,则发生铵根离子与碱的反应,最后沉淀完全溶解,则一定含Al3+,以此来解答.
解答 解:由图可知,开始不生成沉淀,则溶液中一定含H+,然后生成沉淀,一段时间沉淀的量不变,则发生铵根离子与碱的反应,最后沉淀完全溶解,则一定含Al3+,不能含Cu2+、Fe3+、Mg2+、HCO3-,只有D符合,
故选D.
点评 本题考查离子的共存,为高频考点,把握图中沉淀的生成及溶液中离子的判断为解答的关键,侧重分析与应用能力的考查,注意离子反应的先后顺序,题目难度不大.

练习册系列答案
相关题目
13.下列关于实验说法正确是( )
| A. | 氯气可以使湿润的红色布条褪色,所以氯气具有漂白性 | |
| B. | 在配制一定浓度的溶液时未冷却溶液直接将溶液转移至容量瓶中,则浓度偏高 | |
| C. | 因为KNO3的溶解度很大,所以可以用重结晶法除去KNO3中的NaCL杂质 | |
| D. | 向饱和FeCl3溶液中逐滴滴加沸水可以制备Fe(OH)3胶体 |
14.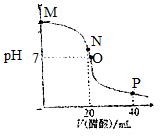 常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )
常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )
 常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )
常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )| A. | N点处恰好完全反应,c(CH3COO-)=c(CH3COOH) | |
| B. | O点处显中性,c(CH3COO-)=c(Na+)=c(H+)=c(OH-) | |
| C. | M点到O点过程中,可能出现c(CH3COO-)>c(Na+) | |
| D. | P点处显酸性,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
11.下列各组离子能在指定溶液中一定能大量共存的是( )
| A. | 饱和氯水中:NH4+、Fe 2+、SO42-、NO3- | |
| B. | pH=1的溶液中:Mg2+、C1-、K+、NO3- | |
| C. | 滴加几滴KSCN溶液变红的溶液中:Na+、NH4+、NO3-、HSO3- | |
| D. | 1.0 mol?L-1的Na2CO3的溶液中:NH4+、SO42-、Cl-、SO2 |
8.将密度为1.2g/cm3的盐酸溶液逐滴滴入到AgNO3溶液中,直到沉淀恰好完全为止,溶液的质量保持不变,则盐酸物质的量浓度为( )
| A. | 25.4% | B. | 50.8% | C. | 6mol/L | D. | 8.36mol/L |
15.用NA表示阿伏加德常数,以下的说法正确的是( )
| A. | 精炼铜时,阳极有1mol物质放电,阴极一定生成NA个铜原子 | |
| B. | 在标准状况下,NA个SO3 分子的质量是80g,其体积就为80/ρ (ρ为SO3的密度) | |
| C. | 1molNaHSO4 熔融液中,其阴阳离子总数目为3NA | |
| D. | PH=1的盐酸溶液中,H+的数目为0.1NA |
下列有关实验操作、现象、解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 用铂丝蘸取某待测液在酒精灯外焰上灼烧 | 呈黄色 | 待测液不含钾元素 |
B | AgBr沉淀中滴入KCl 溶液 | 有白色沉淀出现 | AgCl比AgBr 更难溶 |
C | 铁丝插入稀硝酸中 | 有无色气体产生 | 生成氢气 |
D | 向NaCN溶液中滴加无色酚酞试液 | 溶液变红 | HCN是弱电解质 |
 ,
, .
.