题目内容
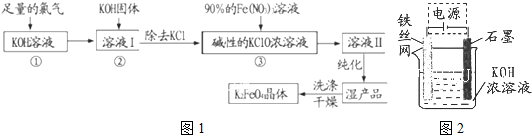
亚铁盐在空气中易被氧化,但形成复盐可稳定存在.硫酸亚铁铵[(NH4)2SO4?FeSO4?6H2O]是一种重要化学试剂,实验室可用纯铁片来制取硫酸亚铁铵,流程如下:
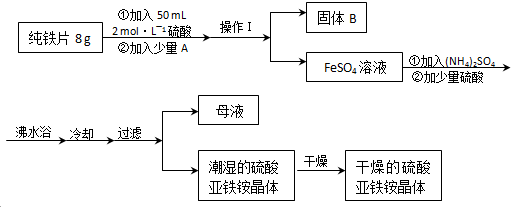
请回答下列问题:
(1)操作Ⅰ的名称是 ,所用主要仪器和用品有(铁架台、铁圈除外) .
(2)若A物质为CuSO4,其加入的目的是 ,则固体B的成分为 .
(3)加少量硫酸可以调节pH为 1~2,其作用是 .

请回答下列问题:
(1)操作Ⅰ的名称是
(2)若A物质为CuSO4,其加入的目的是
(3)加少量硫酸可以调节pH为 1~2,其作用是
考点:制备实验方案的设计,铁的化学性质
专题:几种重要的金属及其化合物
分析:纯铁片加入硫酸中,另外加入硫酸铜,得到硫酸亚铁固体,说明剩余固体中含有铜和单质铁,加入硫酸铜的目的是形成原电池,加快化学反应速率,分类固体和溶液的操作是过滤,调节pH的目的是抑制水解,据此解答各小题即可;
(1)操作Ⅰ是分离固体和液体利用过滤操作进行分离,过滤装置需要的仪器是漏斗、玻璃棒、烧杯、滤纸;
(2)A物质为CuSO4,加入后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行,过滤得到固体为铁和铜;
(3)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,得到更多的产品.
(1)操作Ⅰ是分离固体和液体利用过滤操作进行分离,过滤装置需要的仪器是漏斗、玻璃棒、烧杯、滤纸;
(2)A物质为CuSO4,加入后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行,过滤得到固体为铁和铜;
(3)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,得到更多的产品.
解答:
解:(1)操作Ⅰ是分离固体和液体利用过滤操作进行分离,过滤装置需要的仪器是漏斗、玻璃棒、烧杯、滤纸;故答案为:过滤;漏斗、玻璃棒、烧杯、滤纸;
(2)若A物质为CuSO4,加入后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行,过滤得到固体为铁和铜;故答案为:形成微小原电池,加快铁与硫酸反应速率;Fe和Cu;
(3)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,Fe2++2H2O?Fe (OH)2+2H+; NH4++H2O?NH3?H2O+H+;加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解得到更多的产品;
故答案为:加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解,得到更多的产品.
(2)若A物质为CuSO4,加入后和铁发生反应生成铜析出,和铁在硫酸溶液中形成原电池反应加快反应进行,过滤得到固体为铁和铜;故答案为:形成微小原电池,加快铁与硫酸反应速率;Fe和Cu;
(3)加入少量硫酸可以调节pH为1~2是抑制亚铁离子和铵根离子水解,Fe2++2H2O?Fe (OH)2+2H+; NH4++H2O?NH3?H2O+H+;加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解得到更多的产品;
故答案为:加入硫酸保持酸性,抑制Fe2+、NH4+离子的水解,得到更多的产品.
点评:本题考查了物质制备实验分析判断,物质分离和提纯的方法应用,实验过程分析和物质性质掌握是解题关键他们难道中等.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ?mol-,则氢气的标准燃烧热为-241.8 kJ?mol-11 |
| B、已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| C、已知2C(s)+2O2(g)=2CO2(g)△H=a2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D、已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定 |
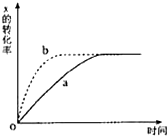 如图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进
如图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
| A、升高温度 |
| B、加大N的投入量 |
| C、缩小体积 |
| D、加大X的投入量 |
下列离子方程式中正确的是( )
| A、碳酸氢钙溶液中加入过量氢氧化钠Ca2-+2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B、氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe2++3H2O |
| C、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O═AlO2-+2NH4++2H2O |
| D、Na2S溶液呈碱性:S2-+H2O=HS-+OH- |