题目内容
下列溶液中微粒的物质的量浓度关系正确的是( )
A.25℃时,pH=7的NH4Cl与NH3·H2O混合溶液:c(H+)= c(OH-)=c(NH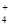 )=c(Cl-)
)=c(Cl-)
B.0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S)
C.25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:
c(HCOO-)+ c(H+)>c(Na+)+c(OH-)
D.0.1mol/LNa2CO3溶液与0.1mol/L NaHCO3溶液等体积混合:2c(CO32-)+2c(HCO3-)+2c(H2CO3)=3c(Na+)
C
【解析】
试题分析:A、25℃时,pH=7的NH4Cl与NH3·H2O混合溶液:c(H+)= c(OH-)< c(NH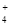 )=c(Cl-),错误;B、根据质子守恒应有c(OH-)=c(H+)+c(HS-)+2c(H2S),错误;C、25℃时,pH=2的HCOOH与pH=12的NaOH相比,HCOOH的浓度大于NaOH的浓度,所以等体积混合后,HCOOH过量,溶液呈酸性,:c(H+)>c(OH-),根据电荷守恒可得c(H+)+c(Na+)= c(HCOO-)+ c(OH-),所以c(HCOO-) >c(Na+),则有
)=c(Cl-),错误;B、根据质子守恒应有c(OH-)=c(H+)+c(HS-)+2c(H2S),错误;C、25℃时,pH=2的HCOOH与pH=12的NaOH相比,HCOOH的浓度大于NaOH的浓度,所以等体积混合后,HCOOH过量,溶液呈酸性,:c(H+)>c(OH-),根据电荷守恒可得c(H+)+c(Na+)= c(HCOO-)+ c(OH-),所以c(HCOO-) >c(Na+),则有
c(HCOO-)+ c(H+)>c(Na+)+c(OH-),正确;D、0.1mol/LNa2CO3溶液与0.1mol/L NaHCO3溶液等体积混合,根据物料守恒得:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+),错误,答案选C。
考点:考查电解质溶液中离子浓度的判断

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
 ,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是( )。
,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是( )。 Cl和
Cl和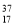 Cl
Cl
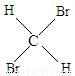 与
与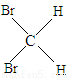

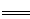 3Fe3++NO↑+3H2O
3Fe3++NO↑+3H2O ===BaSO4↓+H2O
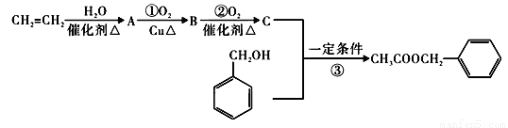
===BaSO4↓+H2O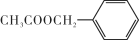 )是其中的一种,它可以从茉莉花中提取。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取。一种合成路线如下: