题目内容
2.某油脂A的分子式CxHyOz,在完全水解后得到三种酸:C17H35COOH、C15H31COOH、C17H33COOH和一种含羟基的有机物B.(1)有机物B的结构简式为HOCH2CH(OH)CH2OH.
(2)0.05mol油脂A完全燃烧得到121g二氧化碳和46.8g水,则x=55;y=104;z=6.
(3)0.05mol油脂A在酸性条件下发生水解,测得油脂A的转化率是40%,除去未水解的油脂A,然后从水解的混合物中提取所得到的四种有机产物组成混合物C,则混合物C最多消耗钠的物质的量是0.18mol.
分析 (1)油脂水解生成羧酸和甘油,则B为甘油;
(2)n(CO2)=$\frac{121g}{44g/mol}$=2.75mol,根据C原子守恒得n(C)=n(CO2)=2.75mol,n(H2O)=$\frac{46.8g}{18g/mol}$=2.6mol,根据H原子守恒得n(H)=2n(H2O)=2×2.6mol=5.2mol,0.05mol油脂A完全燃烧得到121g二氧化碳和46.8g水,即0.05mol油脂A中含有2.75molC、5.2molH原子,则该分子中含有C、H原子个数分别是55、104,一个A分子水解生成三种酸的分子个数之比为1:1:1,A中含有3个酯基,氧原子个数为6;
(3)0.05mol油脂A在酸性条件下发生水解,测得油脂A的转化率是40%,则水解的油脂的物质的量=0.05mol×(1-40%)=0.03mol,0.03molA水解后生成等物质的量的C17H35COOH、C15H31COOH、C17H33COOH和甘油,都是0.03mol,羧基和醇羟基都能和钠反应生成氢气,且-COOH和醇-OH与Na反应的物质的量之比都为1:1.
解答 解:(1)油脂水解生成羧酸和甘油,则B为甘油,其结构简式为HOCH2CH(OH)CH2OH,故答案为:HOCH2CH(OH)CH2OH;
(2)n(CO2)=$\frac{121g}{44g/mol}$=2.75mol,根据C原子守恒得n(C)=n(CO2)=2.75mol,n(H2O)=$\frac{46.8g}{18g/mol}$=2.6mol,根据H原子守恒得n(H)=2n(H2O)=2×2.6mol=5.2mol,0.05mol油脂A完全燃烧得到121g二氧化碳和46.8g水,即0.05mol油脂A中含有2.75molC、5.2molH原子,则该分子中含有C、H原子个数分别是55、104,一个A分子水解生成三种酸的分子个数之比为1:1:1,A中含有3个酯基,氧原子个数为6,则A的分子式为C55H104O6,即x=55、y=104、z=6,
故答案为,55;104;6;
(3)0.05mol油脂A在酸性条件下发生水解,测得油脂A的转化率是40%,则水解的油脂的物质的量=0.05mol×(1-40%)=0.03mol,0.03molA水解后生成等物质的量的C17H35COOH、C15H31COOH、C17H33COOH和甘油,所以C是C17H35COOH、C15H31COOH、C17H33COOH和甘油的混合物,都是0.03mol,羧基和醇羟基都能和钠反应生成氢气,且-COOH和醇-OH与Na反应的物质的量之比都为1:1,0.03molC17H35COOH、C15H31COOH、C17H33COOH和甘油分别和足量钠反应消耗Na的物质的量分别是0.03mol、0.03mol、0.03mol、0.09mol,n(Na)=(0.03×3+0.09)mol=0.18mol,
故答案为:0.18.
点评 本题以油脂为载体考查有机物推断、物质的量有关计算,为高频考点,侧重考查学生分析推断及计算能力,明确各个物理量之间的关系是解本题关键,注意甘油中含有3个醇羟基,题目难度不大.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | 电负性:④>③>②>① | B. | 最高正化合价:③>①>②>④ | ||
| C. | 原子半径:①>②>③>④ | D. | 第一电离能:④>③>②>① |
| A. | X的最高价氧化物对应水化物的酸性大于W | |
| B. | Z的气态氢化物的稳定性大于W | |
| C. | YZ和ZW2所含化学键类型相同 | |
| D. | 简单离子半径:r(Y2+)<r(X-)<r(W-)<r(Z2-) |
| A. | 1mol任何气体都含有相同的原子数 | |
| B. | 1molO2中含有6.02×1023个氧分子 | |
| C. | 1molH2中含有1mol氢原子和2mol电子 | |
| D. | 1molH2SO4中含有6NA个原子 |
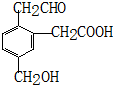 ,它在一定条件下能发生的反应有①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤中和反应 ⑥消去反应( )
,它在一定条件下能发生的反应有①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤中和反应 ⑥消去反应( )| A. | ②③④ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ②③④⑤⑥ |
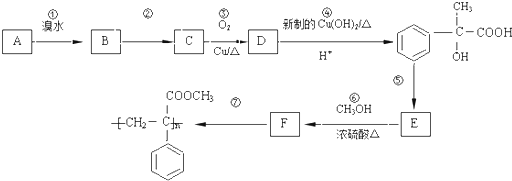
 ,F
,F .
.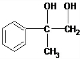 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.
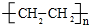 ;
;