题目内容
实验室现需要240mL0.1mol/L的盐酸溶液,准备用密度为1.18g/mL,质量分数为36.5%浓盐酸来配制.填空并请回答下列问题:
(1)配制0.1mol/L的盐酸溶液,应量取浓盐酸体积为 mL.
(2)在容量瓶上无需有的标记是
A.刻度值 B.温度 C.刻度线 D.容量
(3)配制0.1mol/L的盐酸溶液,下列不需用的仪器是:
A.容量瓶 B.托盘天平 C.胶头滴管 D.烧杯
(4)配制时,其正确的操作顺序是(用字母表示,每个字母最多只能用一次) .
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约70mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已溶解好的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,直到液体凹液面的最低点与刻度线相平
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(5)若出现如下情况,对所配溶液浓度将有何影响?(用偏高、偏低、无影响回答.)
没有洗涤烧杯和玻璃棒,并将洗涤液转移到容量瓶中 ;定容时俯视刻度线 ;量取浓盐酸时仰视 .
(1)配制0.1mol/L的盐酸溶液,应量取浓盐酸体积为
(2)在容量瓶上无需有的标记是
A.刻度值 B.温度 C.刻度线 D.容量
(3)配制0.1mol/L的盐酸溶液,下列不需用的仪器是:
A.容量瓶 B.托盘天平 C.胶头滴管 D.烧杯
(4)配制时,其正确的操作顺序是(用字母表示,每个字母最多只能用一次)
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约70mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已溶解好的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,直到液体凹液面的最低点与刻度线相平
F.继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(5)若出现如下情况,对所配溶液浓度将有何影响?(用偏高、偏低、无影响回答.)
没有洗涤烧杯和玻璃棒,并将洗涤液转移到容量瓶中
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:(1)根据c=
计算出浓盐酸的物质的量浓度,配制240mL溶液,需要选用250mL容量瓶,再根据溶液稀释过程中溶质的物质的量不变计算出需要浓盐酸的体积;
(2)根据容量瓶的构造进行解答;
(3)根据配制250mL 0.1mol/L的稀盐酸的步骤选用仪器;
(4)根据配制一定物质的量浓度的溶液方法对各选项进行排序;
(5)根据c=
可得,一定物质的量浓度溶液配制的误差都是由溶质的物质的量n和溶液的体积V引起的,误差分析时,关键要看配制过程中引起n和V怎样的变化:若n比理论值小,或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大,或V比理论值小时,都会使所配溶液浓度偏大.
| 1000ρw |
| M |
(2)根据容量瓶的构造进行解答;
(3)根据配制250mL 0.1mol/L的稀盐酸的步骤选用仪器;
(4)根据配制一定物质的量浓度的溶液方法对各选项进行排序;
(5)根据c=
| n |
| V |
解答:
解:(1)浓盐酸的物质的量浓度为:c=
=
mol/L=11.8mol/L,配制240mL溶液,实验室中没有240mL容量瓶,需要选用250mL的容量瓶进行配制,设所需浓硫酸的体积为V,则有:V×11.8mol/L=O.25L×0.1mol/L,则V=
=O.0021L=2.1mL,
故答案为:2.1;
(2)根据容量瓶的构造可知,容量瓶上标有温度、容量、刻度线,容量瓶上没有具体的刻度值,所以A正确,
故答案为:A;
(3)根据配制步骤可知,配制该溶液需要的仪器为:10mL量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,由于是药品为液体,所以不需要托盘天平,
故答案为:B;
(4)配制一定物质的量浓度的溶液步骤为:量取、稀释、冷却、移液、洗涤、定容、摇匀等操作,所以正确的操作顺序为:BCAFED,
故答案为:BCAFED;
(5)没有进行A操作,烧杯和玻璃棒上都有残留的溶质,没有洗涤烧杯和玻璃棒,会导致溶质的物质的量减少,配制的溶液浓度偏低;
定容时俯视读数,加入的蒸馏水体积偏小,配制的溶液体积偏小,溶液的浓度偏高;
量取浓盐酸时仰视,导致量取的浓盐酸体积偏大,配制的溶液浓度偏高,
故答案为:偏低;偏高;偏高.
| 1000ρw |
| M |
| 1000×1.18×36.5% |
| 36.5 |
| 0.25L×0.1mol/L |
| 11.8mol/L |
故答案为:2.1;
(2)根据容量瓶的构造可知,容量瓶上标有温度、容量、刻度线,容量瓶上没有具体的刻度值,所以A正确,
故答案为:A;
(3)根据配制步骤可知,配制该溶液需要的仪器为:10mL量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,由于是药品为液体,所以不需要托盘天平,
故答案为:B;
(4)配制一定物质的量浓度的溶液步骤为:量取、稀释、冷却、移液、洗涤、定容、摇匀等操作,所以正确的操作顺序为:BCAFED,
故答案为:BCAFED;
(5)没有进行A操作,烧杯和玻璃棒上都有残留的溶质,没有洗涤烧杯和玻璃棒,会导致溶质的物质的量减少,配制的溶液浓度偏低;
定容时俯视读数,加入的蒸馏水体积偏小,配制的溶液体积偏小,溶液的浓度偏高;
量取浓盐酸时仰视,导致量取的浓盐酸体积偏大,配制的溶液浓度偏高,
故答案为:偏低;偏高;偏高.
点评:本题考查了配制一定物质的量浓度的溶液的方法,题目难度中等,试题基础性强,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力.

练习册系列答案
相关题目
下列变化过程,属于放热反应的是( )
①生石灰与水反应
②酸碱中和反应
③浓H2SO4稀释
④固体氢氧化钠溶于水
⑤H2在Cl2中燃烧
⑥醋酸电离
⑦NH4Cl晶体与Ba(OH)2?8H2O混合搅拌
①生石灰与水反应
②酸碱中和反应
③浓H2SO4稀释
④固体氢氧化钠溶于水
⑤H2在Cl2中燃烧
⑥醋酸电离
⑦NH4Cl晶体与Ba(OH)2?8H2O混合搅拌
| A、①②⑤ | B、 ①②③④⑤ |
| C、①③④ | D、⑥⑦ |
下列有关化学用语的使用正确的是( )
A、CH4分子的比例模型: |
B、NH3的电子式: |
C、Cl-的结构示意图: |
| D、CO2的结构式:O=C=O |




 2014年10月初,雾霾天气多次肆虐河北、天津、北京等地区.其中,燃煤和汽车尾气是造成空气污染的原因之一.
2014年10月初,雾霾天气多次肆虐河北、天津、北京等地区.其中,燃煤和汽车尾气是造成空气污染的原因之一.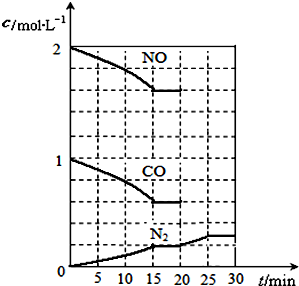 二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.
二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.