题目内容
3.元素X和Y是同周期主族元素,X元素在第ⅠA族,Y元素在第ⅦA族,则X和Y两元素原子序数之差不可能是( )| A. | 6 | B. | 16 | C. | 26 | D. | 30 |
分析 元素X和Y是同周期主族元素,X元素在第ⅠA族,Y元素在第ⅦA族,周期表中第一、二、三、四、五、六、七周期元素的种数分别为2、8、8、18、18、32、32,以此来解答.
解答 解:若元素在二、三周期,则同周期第ⅠA族与第ⅦA族原子序数相差6,
若元素在四、五周期,由于副族和VⅢ族出现在ⅠA和ⅦA族之间,则原子序数相差16,
若元素在第六周期,又多了镧系的出现,有15种元素,则原子序数相差30,
X元素在第ⅠA族,Y元素在第ⅦA族,则X和Y两元素原子序数之差不可能是26,
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握周期表的结构、原子序数的关系为解答的关键,侧重分析与应用能力的考查,注意周期表的族的位置,题目难度不大.

练习册系列答案
相关题目
13.关于下列有机物,说法正确的是( )
| A. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| B. | 按系统命名法, 的名称为4,4-二甲基-3-乙基己烷 的名称为4,4-二甲基-3-乙基己烷 | |
| C. | 满足分子式为C4H8ClBr的有机物有11种 | |
| D. | 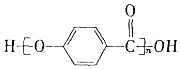 的结构中含有酯基 的结构中含有酯基 |
14.用NA代表阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1.12 L戊烷所含共价键数目为0.8NA | |
| B. | 1 L 0.1 mol/L (NH4)2SO4溶液中含N原子数为0.2NA | |
| C. | 2.2 gD218O与T2O的混合物中所含质子数、中子数均为NA | |
| D. | 一定量的浓硫酸与足量锌共热,产生22.4L气体时,转移的电子数一定为2NA |
11. 英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )
英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )
 英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )
英国科学家发明的尿素微生物电池的反应为:2CO(NH2)2+3O2═2CO2+2N2+4H2O,电池装置如图所示.下列说法正确的是( )| A. | 该装置能够在高温下工作 | |
| B. | 微生物促进了反应中电子的转移 | |
| C. | 装置工作时,电能转变为化学能 | |
| D. | 装置工作时,电子由电极a沿导线流向电极b |
18.下列元素中,最高正化合价数值最大的是( )
| A. | C | B. | F | C. | S | D. | Na |
8.设NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 将1molNH4NO3于稀氨水便溶液呈中性,溶液中NH4+数目为NA | |
| B. | 标准状况下,22.4L甲烷中含有的C-H键数目为3NA | |
| C. | 25℃时,pH=2的硫酸溶液中含有H+的数目为0.01NA | |
| D. | 1molFe与1molCl2充分反应转移电子数为3NA |
15.乙烯是重要的工业原料,下列有关乙烯叙述不正确的是 ( )
| A. | 常温常压下是气体 | B. | 能使溴的四氯化碳溶液褪色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 在一定条件下能够聚合生成聚乙烯 |
12.某种氢氧燃料电池的电解液为KOH溶液,下列有关电池的叙述不正确的是( )
| A. | 负极反应式为:H2+2 OH--2e-═2H2O | |
| B. | 该燃料电池的总反应方程式为:2H2+O2═2H2O | |
| C. | 工作一段时间后,电解液中的KOH的物质的量不变 | |
| D. | 该电池工作时每消耗1mol O2,有2 mol电子转移 |
