题目内容
13.标准状况下4.48L某烯烃和CO的混合气体与足量的氧气混合点燃,使之反应,将反应完毕后生成的气体通过浓硫酸,浓硫酸增重7.2g,并测得剩余气体中CO2为11.2L(标准状况),求此烯烃分子式.分析 根据n=$\frac{V}{{V}_{m}}$、n=$\frac{m}{M}$计算出混合气体、生成二氧化碳、水的物质的量,然后设出烯烃的物质的量为x,则混合气体中含有CO为(0.2-x)mol,根据碳原子守恒、二氧化碳的物质的量列式计算即可.
解答 解:标准状况下混合气体的物质的量为:$\frac{4.48L}{22.4L/mol}$=0.2mol,
浓硫酸增重的为水的质量,其物质的量为:$\frac{7.2g}{18g/mol}$=0.4mol,
烯烃和CO完全燃烧生成的二氧化碳的物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,
设混合气体中含有烯烃的物质的量为x,则含有CO为(0.2-x)mol,
设烯烃的分子式为CnH2n,根据C原子守恒及生成二氧化碳的物质的量可知,nx+(0.2-x)=0.5、nx=0.4,解得:x=0.1、n=4,
则该烯烃的分子式为C4H8,
答:该烯烃分子式为C4H8.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
3.下列各组离子能够大量共存且溶液呈无色的是( )
| A. | K+、Na+、Cl-、CO32- | B. | Mg2+、Al3+、OH-、SO42- | ||
| C. | H+、Ag+、Cl-、SO42- | D. | Fe2+、H+、Na+、NO3- |
18.在五种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③Na2SiO3 ④NaAlO2 ⑤Na2CO3中,分别通入足量的CO2,最终能得到沉淀或析出晶体的是( )
| A. | ②③④ | B. | ①③④ | C. | ②③④ | D. | ③④⑤ |
5.下列括号中的物质是除去杂质所需的药品,其中错误的是( )
| A. | NaCl溶液中有杂质Na2SO4(氯化钡) | B. | FeS04溶液中有杂质CuSO4(铁粉) | ||
| C. | 生石灰中混有少量石灰石(盐酸) | D. | BaCl2溶液中有少量MgCl2(氢氧化钡) |
2.下列说法中错误的是( )
| A. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 | |
| B. | 氯气易液化,液氯可以保存在钢瓶中 | |
| C. | 氯水、氯气、液氯均能与硝酸银溶液反应产生白色沉淀 | |
| D. | 过量的铁在氯气中燃烧生成FeCl2 |
3.两种金属混合粉末15g,与足量的盐酸反应时生成11.2L氢气(标准状况),符合上述情况的金属混合物的是( )
| A. | Mg和Al | B. | Mg和Ag | C. | Na和Zn | D. | Fe和Zn |
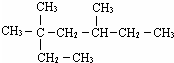 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷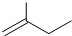 C5H10.
C5H10.