题目内容
钛(Ti)被称为继铁、铝之后的第三金属,以TiO2制取Ti的主要反应有:
①TiO2+2C+2Cl2
TiCl4+2CO,②TiCl4+2Mg
2MgCl2+Ti;下列叙述正确的是( )
①TiO2+2C+2Cl2
| ||
| ||
| A、反应①是复分解反应 |
| B、反应②是置换反应 |
| C、反应①中TiO2是氧化剂 |
| D、反应②中金属镁是氧化剂 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:①TiO2+2C+2Cl2
TiCl4+2CO中,C元素的化合价升高,Cl元素的化合价降低;
②TiCl4+2Mg
2MgCl2+Ti中,Mg元素的化合价升高,Ti元素的化合价降低,以此来解答.
| ||
②TiCl4+2Mg
| ||
解答:
解:A.反应①有单质参加反应,且存在元素的化合价变化,一定不是复分解反应,故A错误;
B.反应②有单质与化合物反应生成新单质与新化合物,是置换反应,故B正确;
C.反应①中,Ti、O元素的化合价不变,则TiO2不是氧化剂,故C错误;
D.反应②中金属镁元素的化合价升高,Mg是还原剂,故D错误;
故选B.
B.反应②有单质与化合物反应生成新单质与新化合物,是置换反应,故B正确;
C.反应①中,Ti、O元素的化合价不变,则TiO2不是氧化剂,故C错误;
D.反应②中金属镁元素的化合价升高,Mg是还原剂,故D错误;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素化合价变化为解答的关键,侧重基本概念的考查,注意元素化合价的判断,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图实验操作装置正确的是( )
A、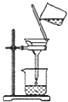 CaCO3的过滤 |
B、 向NaCl溶液中滴加AgNO3溶液 |
C、 硫酸铜晶体的称量 |
D、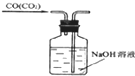 除去水CO中的CO2气体 |
取一定量的镁、铝合金,用足量盐酸溶解后,再加入过量的氢氧化钠溶液,然后滤出沉淀物,加强热灼烧最后得到白色粉末,干燥后称量与原合金的质量相等,则合金中镁的质量百分含量是( )
| A、20% | B、40% |
| C、60% | D、无法计算 |
下列各组离子,能在溶液中大量共存的是( )
| A、Mg2+、Na+、Cl-、OH- |
| B、Na+、H+、OH-、SO32- |
| C、K+、Fe3+、OH-、SO42- |
| D、K+、H+、SO42-、NO3- |
被称为万能还原剂的NaBH4溶于水并和水发生反应:NaBH4+2H2O=NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价)( )
| A、NaBH4是氧化剂,H2O是还原剂 |
| B、被氧化的元素与被还原的元素质量比为1:1 |
| C、硼元素被氧化,氢元素被还原 |
| D、NaBH4既是氧化剂又是还原剂 |
 某同学设计了两种方案制备氢氧化铝.
某同学设计了两种方案制备氢氧化铝.方案一:2.7g Al
| 100mL稀盐酸 |
| NaOH溶液 |
方案二:2.7g Al
| 100mLNaOH溶液 |
| 稀盐酸 |
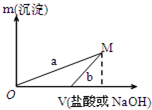
已知所用的稀盐酸与NaOH溶液均为3mol/L.图是向X溶液与Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.相关说法正确的是( )
| A、a曲线表示的是向X溶液中加入NaOH溶液 |
| B、在M点时,两种方案中所得溶液的溶质质量分数相同 |
| C、方案二比方案一生成更多的气体 |
| D、M点以后,a、b两条曲线将重合为一条 |
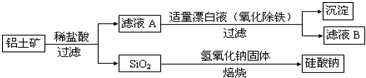
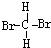 和
和 ⑦
⑦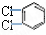 和
和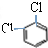 ⑧CH3CH=CHCH2OH和HOCH2CH=CH2
⑧CH3CH=CHCH2OH和HOCH2CH=CH2