题目内容
20.下列有关物质的检验或区分方法中正确的是( )| A. | 向某溶液中加入BaCl2溶液,有白色沉淀,则原溶液一定存在Ag+或SO42- | |
| B. | 向某溶液滴加NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,可确定原溶液中无NH4+ | |
| C. | 向某溶液中加入足量的盐酸,放出二氧化碳气体,可证明该溶液中一定含有碳酸盐 | |
| D. | 用洁净铁丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液中有Na+ |
分析 A.向某溶液中加入BaCl2溶液,有白色沉淀,可生成碳酸钡等;
B.氨气易溶于水,生成氨气不一定从溶液析出;
C.也可能为碳酸氢盐;
D.钠元素的焰色反应为黄色.
解答 解:A.向某溶液中加入BaCl2溶液,有白色沉淀,可生成碳酸钡等,原溶液不一定存在Ag+或SO42-,故A错误;
B.氨气易溶于水,生成氨气不一定从溶液析出,应进行加热等操作,且浓度较大,故B错误;
C.生成二氧化碳,也可能为碳酸氢盐,不一定为碳酸盐,故C错误;
D.钠元素的焰色反应为黄色,火焰呈黄色,则原溶液中有Na+,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应及物质鉴别方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
10.用下列实验装置和方法进行相应实验,正确的是( )
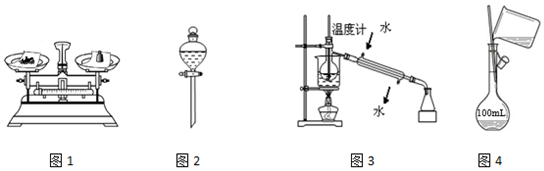

| A. | 用图1所示方法称量固体氯化钠 | |
| B. | 用图2装置分离碘的四氯化碳溶液 | |
| C. | 用图3所示装置和方法进行石油分馏 | |
| D. | 用图4装置配制150 mL稀盐酸 |
11.某无色强酸性溶液中能大量共存的离子组是( )
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、NO3-、SO42-、I- | ||
| C. | Na+、K+、Cl-、S2- | D. | Fe3+、K+、Cl-、SO42- |
8.下列关于钠及其化合物的说法错误的是( )
| A. | 钠着火时可用细砂来灭火 | |
| B. | 切开的金属钠暴露在空气中,光亮的表面变暗发生2Na+O2═Na2O2反应 | |
| C. | 过氧化钠在潮湿空气放一段时间变成白色粘稠物的反应主要是:2Na2O2+2H2O═4NaOH+O2↑ | |
| D. | 过氧化钠投入硫酸铜溶液可产生氢氧化铜沉淀和氧气 |
15.如果NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | NA个CO2分子中含1mol氧原子 | |
| B. | 3.2g S2-的核外电子数1.6NA | |
| C. | 1 mol•L-1Na2CO3溶液中含有2NA个Na+ | |
| D. | 1个H2SO4分子中氧原子的质量为64/NAg |
5.在一定温度下的某容积不变的密闭容器中,建立下列化学平衡C(s)+H2O(g)?CO(g)+H2(g),不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | v正(H2O)=v正(H2) | |
| B. | V正(CO)=V逆(H2O) | |
| C. | 生成nmolCO的同时生成nmolH2O | |
| D. | 1 molH-H键断裂的同时断裂2molH-O键 |
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O=HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2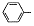 +CO2+H2O→2 +CO2+H2O→2 OH+CO32- OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
13.下列说法不正确的是( )
| A. | 向滴有酚酞的水中加入过量Na2O2粉末并振荡,溶液由无色变红又变无色 | |
| B. | 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界 | |
| C. | 将一小粒金属钠投入水和苯的混合体系中,钠在苯与水的界面处反应并可能作上、下跳动 | |
| D. | 某物质灼烧时,焰色反应为黄色,该物质一定只含钠元素 |