题目内容
由某饱和一元醛和饱和一元酮组成的混合物共0.5mol,其质量为23.4g,此混合物与足量银氨溶液反应析出86.4g银,推断混合物的组成.
考点:有关有机物分子式确定的计算
专题:
分析:由某饱和一元醛和饱和一元酮组成的混合物共0.5mol,其质量为23.4g,混合物的平均摩尔质量为:
=46.8g,饱和一元酮碳原子数最小的为并同,相对分子质量为58,故相对分子质量小于46.8的为醛类;可能为甲醛或乙醛;析出银的物质的量为:
=0.8mol,若是乙醛,则R-CHO~2Ag,假设饱和一元醛是甲醛,则H-CHO~4Ag,计算出酮的摩尔质量,进而确定混合物的组成.
| 23.4g |
| 0.5mol |
| 86.4g |
| 108g/mol |
解答:
解:由某饱和一元醛和饱和一元酮组成的混合物共0.5mol,其质量为23.4g,混合物的平均摩尔质量为:
=46.8g,饱和一元酮碳原子数最小的为丙酮,相对分子质量为58,故相对分子质量小于46.8的为醛类;可能为甲醛或乙醛;析出银的物质的量为:
=0.8mol,若是乙醛,则R-CHO~2Ag,则乙醛的物质的量为0.4mol,质量为:0.4mol×44g/mol=17.6g,则酮的物质的量为0.5mol-0.4mol=0.1mol,酮的质量为:23.4g-17.6g=5.8g,则酮的摩尔质量为:
=58g/mol,故为丙酮;假设饱和一元醛是甲醛,则H-CHO~4Ag,则甲醛的物质的量为0.2mol,质量为:0.2mol×30g/mol=6.0g,酮的物质的量为0.5mol-0.2mol=0.3mol,酮的质量为:23.4g-6.0g=17.4g,酮的摩尔质量为:
=58g/mol,故为丙酮;
答:混合物为0.4mol乙醛和0.1mol丙酮混合物或为0.2mol甲醛和0.3mol丙酮混合物.
| 23.4g |
| 0.5mol |
| 86.4g |
| 108g/mol |
| 5.8g |
| 0.1mol |
| 17.4g |
| 0.3mol |
答:混合物为0.4mol乙醛和0.1mol丙酮混合物或为0.2mol甲醛和0.3mol丙酮混合物.
点评:本题考查有机物推断,属于计算型推断,难度中等,侧重考查学生分析解决问题能力,注意利用假设法进行解答,注意理解甲醛与银氨溶液反应.

练习册系列答案
相关题目
BaCl2剧毒,致死量为0.3g,万一不慎误服,应按第7题的处理外,还应服用适量解毒剂,此解毒剂应是( )
| A、AgNO3 |
| B、CuSO4 |
| C、Na2CO3 |
| D、MgSO4 |
下列反应的离子方程式书写正确的是( )
| A、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | ||
B、金属铝溶于氢氧化钠溶液:Al+2OH-=AlO
| ||
| C、金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ | ||
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
下列物质的分类合理的是( )
| A、氧化物:CO2 NO SO2 H2O |
| B、碱:NaOH KOH Ba(OH)2 Na2CO3 |
| C、铵盐:NH4Cl NH4NO3 (NH4)2SO4 NH3?H2O |
| D、酸:NaHSO3 HCl H2SO4 HNO3 |
下列含有相同元素的化合物组是( )
| A、O2、O3 |
| B、CO、CO2 |
| C、KCl、AlCl3 |
| D、NaHCO3、NaHSO4 |
海战中常使用烟草弹是由液氨、SiCl4等物质混合物.用粗硅和氯气通过加热制得的SiCl4中往往含有FeCl3、AlCl、PCl5等杂质,已知SiCl4、FeCl3、AlCl、PCl5等都是极易发生水解反应.下列有关说法正确的是( )
| A、浓烟主要是由生成的大量NH4Cl造成的 |
| B、以上物质的水解都生成对应的酸和碱 |
| C、CCl4和SiCl4的分子结构相似,故CCl4也容易发生水解 |
| D、NH3属于弱电解质 |
如图所示的钢铁腐蚀中下列说法正确的是( )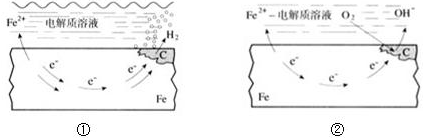

| A、碳表面发生氧化反应 |
| B、钢铁被腐蚀的最终产物为FeO |
| C、生活中钢铁制品的腐蚀以图①所示为主 |
| D、图②中,正极反应式为O2+4e-+2H2O═4OH- |