题目内容
5.下列各溶液中,Na+浓度最大的是( )| A. | 0.5L1.2mol•L-1的Na2SO4溶液 | B. | 2L 0.8mol•L-1的Na0H溶液 | ||
| C. | 1L1mol•L-1的Na2CO3溶液 | D. | 4L 0.5mol•L-1的NaCl溶液 |
分析 电解质溶液中离子浓度=电解质浓度×化学式中相应离子数目,与溶液体积无关.
解答 解:A.0.5L 1.2mol•L-1的Na2SO4溶液中Na+浓度为2×1.2mol/L=2.4mol/L;
B.2L 0.8mol•L-1的NaOH溶液中Na+浓度为1×0.8mol/L=0.8mol/L;
C.1L 1mol•L-1的Na2CO3溶液中Na+浓度为2×1mol/L=2mol/L;
D.4L 0.5mol•L-1的NaCl溶液中Na+浓度为1×0.5mol/L=0.5mol/L,
故选:A.
点评 本题考查物质的量浓度有关计算,比较基础,注意根据电离方程式理解电解质浓度与离子浓度关系.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
15.有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06g Na2CO3和0.84gNaHCO3,A、B中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
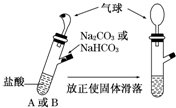

| A. | A装置的气球膨胀速度快 | |
| B. | 若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L | |
| C. | 若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L | |
| D. | 最终两试管中Na+的物质的量一定相同 |
13.已知FeCl3溶液与KSCN溶液混合后发生反应FeCl3+3KSCN?Fe(SCN)3+3KCl,达到平衡后,改变条件,则下列说法正确的是( )
| A. | 向溶液中加入少许KCl固体,溶液颜色变浅 | |
| B. | 升高温度,平衡一定发生移动 | |
| C. | 加入少许KCl固体或者加入少许FeCl3固体平衡常数均发生变化,且变化方向相反 | |
| D. | 平衡常数表达式为K=$\frac{c[Fe(SCN)_{3}]•{c}^{3}(KCl)}{c(FeC{l}_{3})•{c}^{3}(KSCN)}$ |
20.NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 37gNH4F和16gCH4中含有的共价键数均为4NA | |
| B. | 0.51.4mol•L-1的NaHSO3溶液中含有的SO32-数为2NA | |
| C. | 标准状况下,16.8LNO2完全溶于水,转移电子数为0.5NA | |
| D. | 高温高压和催化剂条件下,密闭容器中2gH2与足量N2反应,转移电子数为2NA |
17.有4种混合溶液,分别由等体积等物质的量浓度的2种溶液混合而成,①NH4Cl与HCl;②NH4Cl与NaOH;③NH4Cl与NaCl;④NH4Cl与AlCl3,下列说法正确的是( )
| A. | c(NH4+):②>④>③>① | B. | pH:②>③>④>① | ||
| C. | c(H+):①>③>②>④ | D. | c(NH3•H2O):②>④>③>① |
14.钾.钠合金(含50%~80%钾),可作原子反应堆的导热剂,下面有关该合金的事实与此应用无关的是( )
| A. | 熔点260.7K | B. | 具有很高的比热 | C. | 可作冷却剂 | D. | 能跟水剧烈反应 |