题目内容
下列离子方程式与所述事实相符且正确的是( )
| A、Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| B、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O |
| C、向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| D、明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-=2BaSO4↓+Al(OH)3↓ |
考点:离子方程式的书写
专题:元素周期律与元素周期表专题
分析:A.碳酸氢钙与少量的氢氧化钠反应生成碳酸钙,碳酸氢钠和水;
B.磁性氧化铁为四氧化三铁,与稀硝酸反应生成硝酸铁和水;
C.二价铁离子的还原性强于溴离子,氯气先氧化二价铁离子,然后再氧化溴离子;
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀生成硫酸钡和偏铝酸钠和水.
B.磁性氧化铁为四氧化三铁,与稀硝酸反应生成硝酸铁和水;
C.二价铁离子的还原性强于溴离子,氯气先氧化二价铁离子,然后再氧化溴离子;
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀生成硫酸钡和偏铝酸钠和水.
解答:
解:A.Ca(HCO3)2溶液中加入少量NaOH溶液,离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H2O,故A错误;
B.磁性氧化铁溶于稀硝酸,离子方程式:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故B错误;
C.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应,离子方程式为:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2,故C正确;
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀的离子方程式为Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O,故D错误;
故选:C.
B.磁性氧化铁溶于稀硝酸,离子方程式:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故B错误;
C.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应,离子方程式为:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2,故C正确;
D.明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀的离子方程式为Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,掌握离子方程式书写的方法是解题关键,注意反应物用量对反应的影响,D为易错选项.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在某稀溶液中含有0.1mol HNO3和0.1mol H2SO4,向其中加入9.6g铜粉,充分反应后产生的气体在标准状况下的体积( )
| A、1.12 L |
| B、1.68 L |
| C、2.24 L |
| D、3.36 L |
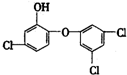 据报道,某牙膏中含有的消毒剂三氯生,遇含氯的自来水会生成哥罗芳(三氯甲烷),哥罗芳能导致肝病,甚至癌症.已知三氯生的结构简式如图所示,下列有关说法中不正确的是( )
据报道,某牙膏中含有的消毒剂三氯生,遇含氯的自来水会生成哥罗芳(三氯甲烷),哥罗芳能导致肝病,甚至癌症.已知三氯生的结构简式如图所示,下列有关说法中不正确的是( )| A、三氯生能与NaOH反应 |
| B、三氯生是一种芳香族化合物 |
| C、三氯生与NaHCO3作用可产生CO2气体 |
| D、哥罗芳没有同分异构体 |
在一定条件下,既能发生氧化反应,又能发生还原反应的是( )
①乙醇 ②乙醛 ③乙酸 ④葡萄糖.
①乙醇 ②乙醛 ③乙酸 ④葡萄糖.
| A、只有①②④ | B、只有② |
| C、只有②④ | D、只有③④ |
下列叙述正确的是( )
| A、常温下干燥的Cl2能用钢瓶贮存 |
| B、14C可用于文物的年代鉴定,14C与12C互为同素异形体 |
| C、BaSO4 在医学上用作钡餐,Ba2+对人体无毒 |
| D、煤的干馏和石油的分馏均属化学变化 |
下列说法正确的是( )
| A、若配制100mL 0.5mol/L Na2SO4溶液,则需要称量Na2SO4?10H2O的质量为7.1g |
| B、80g NaOH溶于1L水中,则溶质的物质的量浓度为2mol/L |
| C、1mol氢气和1mol氦气中,所含的分子数相同、原子数相同、质量也相同 |
| D、1mol Al与足量的稀盐酸反应,失去的电子数为3NA |
氯气是一种化学性质很活泼的非金属单质,下列叙述中不正确的是( )
| A、红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| B、钠在氯气中燃烧,生成白色的烟 |
| C、氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
| D、铁在氯气中燃烧和铁与盐酸反应生成的氯化物是一样的 |
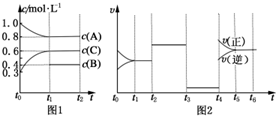 向体积为2L的密闭容器中充入2mol A、0.6mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g)?3C(g)△H>0,各物质的浓度随时间变化的关系如图1所示,其中t0~t1阶段c(B)未画出.图2为反应体系中反应速率随时间变化的情况,且t2,t3,t4各改变一种不同的条件.
向体积为2L的密闭容器中充入2mol A、0.6mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g)?3C(g)△H>0,各物质的浓度随时间变化的关系如图1所示,其中t0~t1阶段c(B)未画出.图2为反应体系中反应速率随时间变化的情况,且t2,t3,t4各改变一种不同的条件.