题目内容
2.下列事实与共价键的强弱有关的是( )| A. | HF的沸点高于HCl | B. | 金刚石的熔点比晶体硅高 | ||
| C. | 稀有气体一般很难发生化学反应 | D. | 常温下单质溴呈液态、碘呈固态 |
分析 A.分子晶体的沸点与分子间作用力有关;
B.原子晶体的熔点与共价键有关;
C.稀有气体原子的电子排布为稳定结构;
D.分子晶体的熔沸点与分子间作用力有关.
解答 解:A.HF分子之间存在氢键,HCl分子间存在范德华力,氢键的作用力大于范德华力,所以HF的沸点高于HCl,故A不选;
B.原子晶体的熔点与共价键有关,原子半径越小,共价键键能越大,原子晶体的熔点越高,所以金刚石的熔点比晶体硅高,故B选;
C.稀有气体原子的电子排布为稳定结构,不容易得失电子,所以一般很难发生化学反应,故C不选;
D.单质溴中分子间作用力小于单质碘中分子间作用力,单质溴的熔点低于单质碘,因此常温下单质溴呈液态、碘呈固态,故D不选.
故选B.
点评 本题考查晶体的熔沸点的比较以及化学键知识,侧重于学生的分析能力和基础知识的综合运用,难度不大,注意基础知识的考查.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
13.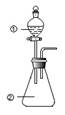 向如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
向如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
 向如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
向如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( ) | 选项 | ① | ② | 现象 |
| A | 浓盐酸 | 二氧化锰 | 产生黄绿色气体 |
| B | 氯化铁溶液 | 铁氰化钾溶液 | 产生蓝色沉淀 |
| C | 浓硝酸 | 用砂纸打磨过的铝条 | 无明显现象 |
| D | 偏铝酸钠 | 稀盐酸 | 立即产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
10.反应 PCl5(g)?PCl3(g)+Cl2(g) ①2HI(g)?H2(g)+I2(g)②在一定条件下,达到化学平衡时,反应物的转化率均是 a%.若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率( )
| A. | 均增大 | B. | 均不变 | C. | ①增大,②不变 | D. | ①减小,②不变 |
17.在100mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.3mol•L-1、0.15mol•L-1,向该混合液中加入2.56g铜粉,加热,待充分反应后,所得溶液中铜离子的物质的量浓度是( )
| A. | 0.15 mol•L-1 | B. | 0.225 mol•L-1 | C. | 0.30 mol•L-1 | D. | 0.45 mol•L-1 |
7.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 配制CuSO4溶液 | 将硫酸铜晶体溶于热水中,然后稀释 |
| B | 除去试管内壁的银镜 | 加入浓氨水浸泡,再用蒸馏水洗涤 |
| C | 提纯含少量乙酸的乙醇(乙醇沸点78.5℃) | 加入生石灰后进行蒸馏,收集78.5℃馏分 |
| D | 证明HClO为弱酸 | 用洁净的玻璃棒蘸取NaClO溶液在pH试纸上,待试纸变色后与标准比色对照 |
| A. | A | B. | B | C. | C | D. | D |
14.以下有关钠的化合价的叙述中.正确的是( )
| A. | Na2O属于碱性氧化物 | |
| B. | Na2CO3长期暴露在空气中变为NaHCO3 | |
| C. | NaOH溶液保存在带玻璃塞的玻璃瓶中 | |
| D. | 向NaHCO3溶液中滴加稀盐酸,开始时无想象,一段时间后有气泡产生 |
11.氮元素可形成卤化物,叠氮化物及配合物等许多化合物.下列说法不正确的是( )
| A. | NF3分子的空间构型为三角锥形 | |
| B. | 叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-,则N2O与N3-互为等电子体 | |
| C. | 叠氮化物与Co3+等形成配合物,如:[Co(N3)(NH3)5]SO4,则其中钴的配位数为8 | |
| D. | NaN3与KN3的结构类似,则NaN3的晶格能大于KN3的晶格能 |
7.下列有关描述中正确的是( )
| A. | 牺牲阳极的阴极保护法是应用电解原理防止金属的腐蚀 | |
| B. | AlCl3溶液和Al2(SO4)3溶液分别加热蒸发,所得固体的成分相同 | |
| C. | 室温时将Na2CO3溶液加水稀释后,再恢复至室温,pH和KW均减小 | |
| D. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol |