题目内容
(1)如图所示,反应2SO2(g)+O2(g)?2SO3(g);△H<0,在不同温度、不同压强(P1>P2)下达到平衡时,混合气中SO3的体积分数φ(SO3)
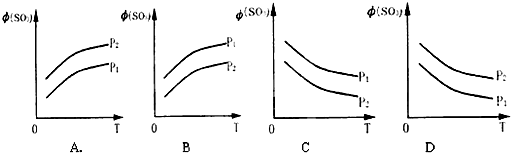
随温度变化的曲线为(填选项字母)
(2)在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol?L-1,试求:
①x值为
②此温度下平衡常数K为
③A的转化率为
④用A表示的化学反应速率为 .

随温度变化的曲线为(填选项字母)
(2)在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol?L-1,试求:
①x值为
②此温度下平衡常数K为
③A的转化率为
④用A表示的化学反应速率为
考点:产物的百分含量随浓度、时间的变化曲线,化学平衡的影响因素
专题:化学平衡专题
分析:(1)对于反应2SO2(g)+O2(g)?2SO3(g);△H<0,正反应是体积减小的放热反应,升高温度平衡向逆反应移动,SO3的体积φ(SO3)减小;增大压强平衡向正反应移动,SO3的体积φ(SO3)增大,依此进行判断;
(2)①根据n=cV计算生成的C的物质的量,利用物质的量之比等于化学计量数之比计算x值;
②利用三段式计算出平衡时各组分的平衡浓度,代入平衡常数表达式计算;
③利用方程式计算参加反应的A的物质的量,再根据转化率定义计算A的转化率;
④关键v=
进行计算.
(2)①根据n=cV计算生成的C的物质的量,利用物质的量之比等于化学计量数之比计算x值;
②利用三段式计算出平衡时各组分的平衡浓度,代入平衡常数表达式计算;
③利用方程式计算参加反应的A的物质的量,再根据转化率定义计算A的转化率;
④关键v=
| △c |
| △t |
解答:
解:(1)对于反应2SO2(g)+O2(g)?2SO3(g);△H<0,正反应是体积减小的放热反应,升高温度平衡向逆反应移动,SO3的体积φ(SO3)减小;增大压强平衡向正反应移动,SO3的体积φ(SO3)增大.
A.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越大;温度一定时,压强越高,SO3的体积φ(SO3)越小,与实际不符合,故A错误;
B.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越大;温度一定时,压强越高,SO3的体积φ(SO3)越大,与实际不符合,故B错误;
C.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越小;温度一定时,压强越高,SO3的体积φ(SO3)越大,与实际相符,故C正确;
D.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越小;温度一定时,压强越高,SO3的体积φ(SO3)越小,与实际不符合,故D错误;
故答案为:C;
(2)①平衡时C的浓度为0.4mol/L,故生成C的物质的量为0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,故0.8mol:0.8mol=x:2,解得x=2,
故答案为:2;
②平衡时C的浓度为0.4mol/L,则:
3A(g)+B(g)?2C(g)+2D(g)
开始(mol/L):1 1 0 0
变化(mol/L):0.6 0.2 0.4 0.4
平衡(mol/L):0.4 0.8 0.4 0.4
故该温度下,该反应的平衡常数k=
=
=0.5,
故答案为:0.5;
③平衡时生成0.8molD,故参加反应的A的物质的量为0.8mol×
=1.2mol,故A的转化率为
×100%=60%,
故答案为:60%;
④v(A)=
=0.3 mol?L-1?min-1,故答案为:0.3 mol?L-1?min-1.
A.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越大;温度一定时,压强越高,SO3的体积φ(SO3)越小,与实际不符合,故A错误;
B.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越大;温度一定时,压强越高,SO3的体积φ(SO3)越大,与实际不符合,故B错误;
C.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越小;温度一定时,压强越高,SO3的体积φ(SO3)越大,与实际相符,故C正确;
D.由图象可知,压强一定时,温度越高,SO3的体积φ(SO3)越小;温度一定时,压强越高,SO3的体积φ(SO3)越小,与实际不符合,故D错误;
故答案为:C;
(2)①平衡时C的浓度为0.4mol/L,故生成C的物质的量为0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,故0.8mol:0.8mol=x:2,解得x=2,
故答案为:2;
②平衡时C的浓度为0.4mol/L,则:
3A(g)+B(g)?2C(g)+2D(g)
开始(mol/L):1 1 0 0
变化(mol/L):0.6 0.2 0.4 0.4
平衡(mol/L):0.4 0.8 0.4 0.4
故该温度下,该反应的平衡常数k=
| c2(C)?c2(D) |
| c3(A)?c(B) |
| 0.42×0.42 |
| 0.43×0.8 |
故答案为:0.5;
③平衡时生成0.8molD,故参加反应的A的物质的量为0.8mol×
| 3 |
| 2 |
| 1.2 |
| 2 |
故答案为:60%;
④v(A)=
| ||
| 2min |
点评:本题考查化学平衡图象、影响化学平衡的因素、化学平衡的有关计算等知识,难度中等.

练习册系列答案
相关题目
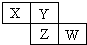 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )| A、氢化物的稳定性:X>Y |
| B、W的最高价氧化物对应水化物的酸性比Z的强 |
| C、Y的非金属性比X的强 |
| D、Y与Z形成的化合物是形成酸雨的主要物质 |
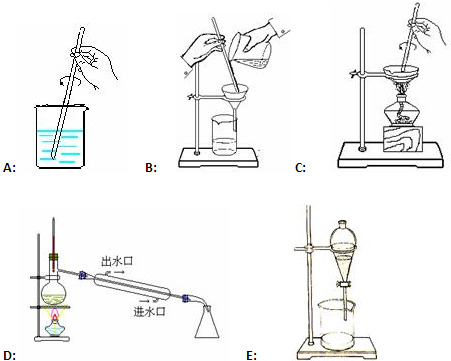
 (3)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是
(3)本实验用到的基本仪器已有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是