题目内容
16.下列各组离子在通入SO2前后均能大量共存的是( )| A. | Fe3+、Al3+、Br-、SO42- | B. | Na+、K+、OH-、SiO32- | ||
| C. | Ca2+、K+、Br-、Cl- | D. | Li+、H+、NO3-、SO42- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,并结合通入SO2不反应来解答.
解答 解:A.该组离子之间不反应,可大量共存,且通入SO2与Fe3+发生氧化还原反应,不能共存,故A不选;
B.该组离子之间不反应,可大量共存,且通入SO2与OH-、SiO32-发生复分解反应,不能共存,故B不选;
C.该组离子之间不反应,可大量共存,且通入SO2不发生反应,可大量共存,故C选;
D.该组离子之间不反应,可大量共存,且通入SO2与H+、NO3-发生氧化还原反应,不能共存,故D不选;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
7.反应A(g)+3B(g)?2C(g)在2L密闭容器中反应,0.5min内C的物质的量增加了0.6mol有关反应速率中正确的是( )
| A. | v(A)=0.005mol•L-1•s-1 | B. | v(C)=0.02mol•L-1•s-1 | ||
| C. | v(B)=$\frac{v(A)}{3}$ | D. | v(A)=0.01mol•L-1•s-1 |
4.如图装置在化学工业中有广泛应用.X、Y是两块石墨,通过导线与直流电源相连.下列说法错误的( )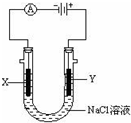

| A. | 该装置发生了化学变化 | B. | 该装置可获得氯气 | ||
| C. | 该装置可获得金属钠 | D. | 溶液中的Na+向X极移动 |
1.下列说法正确的是( )
| A. | 1molO2的质量是32g•mol-1 | |
| B. | H2的摩尔质量是2g | |
| C. | 1molH+的质量是1g | |
| D. | 对原子而言,摩尔质量就是相对原子质量 |
8.短周期元素X、Y、Z、W的原子序数依次增大,X是形成化合物很多的元素,且X常见化合价为+1和-1,Y原子最外层电子数是次外层的3倍;Z与X处于同一主族,W的原子序数是Y的2倍.下列叙述不正确的是( )
| A. | 原子半径的大小顺序:r(Z)>r(W)>r(Y)>r(X) | |
| B. | 元素Y的简单气态氢化物的热稳定性比W的弱 | |
| C. | 化合物Z2Y2与X2Y反应时,Z2Y2既是氧化剂又是还原剂 | |
| D. | 由X、Y、Z、W四种元素组成的两种化合物不能发生化学反应 |
5.向一固定体积的密闭容器中通入a mol N2O4气体,在密闭容器内发生反应:N2O4(g)?2NO2(g),达到平衡时再通入a mol N2O4气体,再次达到平衡时,与第一次达平衡时相比,N2O4的转化率( )
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
6.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学设计了如下实验方案并验证产物、探究反应原理.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
(3)为进一步确定实验1的产物,设计定量实验方案,如图所示: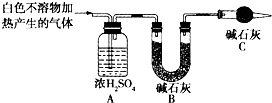
称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 ;
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行.
(1)提出假设
实验1:用砂纸擦去镁条表面的氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变为红.该同学对反应中产生的白色不溶物进行如下猜测:
猜测1:白色不溶物可能为Mg(OH)2;
猜测2:白色不溶物可能为MgCO3.
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3•yMg(OH)2].
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | 气体成分为 ①氢气 |
| 实验Ⅲ | 取实验Ⅰ中的白色不溶物,洗涤,加入足量 ②稀盐酸 | ③产生气泡沉淀全部溶解 | 白色不溶物可能含有猜测2中不溶物 |
| 实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | 溶液中存在 ④CO32- |

称取实验1中所得干燥、纯净的白色不溶物22.6g,充分加热至不再产生气体为止,并使分解产生的气体全部通入装置A和B中.实验后装置A增重1.8g,装置B增重8.8g,试确定白色不溶物的化学式:Mg(OH)2(CO3)2或2MgCO3•Mg(OH)2 ;
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:NaHCO3溶液中存在平衡,HCO3-?H++CO32-、H2O?H++OH-;Mg和H+反应生成氢气和镁离子,镁离子和氢氧根离子、碳酸根离子反应生成难溶物Mg(OH)2•2MgCO3,则H+、OH-、CO32-的浓度均减小,促使上述两平衡均向右进行.