题目内容
3.下列关于铜及其化合物的说法中正确的是( )| A. | 在铜的精炼中,粗铜为阳极 | |
| B. | 铜在空气中也容易生锈,可用稀硝酸洗涤 | |
| C. | 铜离子氧化性较强,能氧化I-,所以Cu2+与S2-反应将生成硫单质 | |
| D. | 铜金属性比铁弱,因此Cu2+与铁反应生成Fe3+ |
分析 A.粗铜为阳极,失去电子,纯铜为阴极;
B.Cu与硝酸反应;
C.CuS为难溶电解质;
D.Cu2+与铁发生置换反应生成亚铁离子、Cu.
解答 解:A.在铜的精炼中,粗铜为阳极,失去电子,纯铜为阴极,阳极上活泼金属Zn、Fe及Cu失去电子,不活泼金属形成阳极泥,阴极上只有铜离子得到电子,故A正确;
B.Cu与硝酸反应,则Cu不能利用硝酸洗涤,应选盐酸洗涤,故B错误;
C.铜离子氧化性较强,能氧化I-,但CuS为难溶电解质,Cu2+与S2-反应生成CuS,故C错误;
D.铜金属性比铁弱,Cu2+与铁发生置换反应生成亚铁离子、Cu,故D错误;
故选A.
点评 本题考查铜及其化合物的性质、电解应用及氧化还原反应,为高频考点,把握物质的性质、反应原理等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
14.胶体区别于其它分散系的本质特征是( )
| A. | 胶体能发生电泳现象 | B. | 胶体能产生丁达尔现象 | ||
| C. | 胶体粒子直径在1~100nm之间 | D. | 胶体在一定条件下能聚沉 |
18.化学与生产、生活、社会密切相关,下列有关说法中正确的是( )
| A. | 2014年1月,国家首次将雾霾天气纳入自然灾情进行通报,雾霾是一种不同于胶体的分散系,它的形成与大量焚烧田间秸秆有关 | |
| B. | 纤维素和淀粉一样可水解成葡萄糖,因此人类可从中获得生存所需的能量 | |
| C. | 2015年诺贝尔化学奖授予从分子水平揭示细胞如何修复损伤DNA以及保护遗传信息的三位科学家,DNA水解产物为氨基酸 | |
| D. | 陶瓷刀号称贵族刀,作为现代高科技的产物,大多是用一种纳米材料“氧化锆”为原料加工而成,具有硬度高、导热性好、抗腐蚀等优点 |
8.A、B、C、X是中学化学常见物质,转化关系如图所示,则有关说法不正确的是( )


| A. | 若A是金属铁,则B溶液可使酸性高锰酸钾溶液褪色 | |
| B. | 若A、B、C中均含同一种常见金属元素,且该元素在C中以阴离子形式存在,则A溶液与C溶液可发生反应生成白色沉淀 | |
| C. | 若A、B、C的焰色反应均呈黄色,水溶液均为碱性,则X不可能为直线形分子 | |
| D. | 若A为固态非金属单质,A与X同周期,则C中所有原子可能都满足8电子结构 |
15.在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如图所示,试回答下列问题:
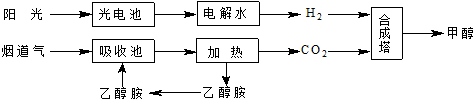
(1)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,图示合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-.
(2)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-131.9kJ/mol.
(3)500℃时,密闭容器中充入1mol/L CO2和3mol/LH2发生反应:
CO2(g)+3H2(g)$?_{高温高压}^{催化剂}$CH3OH(g)+H2O(g)
测得有关数据如表:
计算该反应的平衡常数K(保留一位小数)5.3;
(4)以渗透于多孔基质的惰性导电物材料为电极,用35~50%KOH为电解液,甲醇和空气为原料,构成碱性燃料电池.请写电极反应
正极:O2+4e-+2H2O=4OH-,负极:2CH3OH-12e-+16OH-=2CO32-+12H2O.
(5)合成甲醇的另一种反应是:CO(g)+2H2(g)?CH3OH(g),试分析此反应是放热(填“放热”或“吸热”)反应.对已达平衡此反应在保证氢气浓度不变的情况下,增大容器的体积,平衡B移动;
A.正向移动 B.不移动 C.逆向移动 D.不一定.

(1)15~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,图示合成线路中用作CO2吸收剂.用离子方程式表示乙醇胺水溶液呈弱碱性的原因HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-.
(2)CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-131.9kJ/mol.
(3)500℃时,密闭容器中充入1mol/L CO2和3mol/LH2发生反应:
CO2(g)+3H2(g)$?_{高温高压}^{催化剂}$CH3OH(g)+H2O(g)
测得有关数据如表:
| 反应时间/min | 3 | 5 | 7 | 10 | 13 |
| c(CO2)/mol•L-1 | 0.50 | 0.37 | 0.30 | 0.25 | 0.25 |
(4)以渗透于多孔基质的惰性导电物材料为电极,用35~50%KOH为电解液,甲醇和空气为原料,构成碱性燃料电池.请写电极反应
正极:O2+4e-+2H2O=4OH-,负极:2CH3OH-12e-+16OH-=2CO32-+12H2O.
(5)合成甲醇的另一种反应是:CO(g)+2H2(g)?CH3OH(g),试分析此反应是放热(填“放热”或“吸热”)反应.对已达平衡此反应在保证氢气浓度不变的情况下,增大容器的体积,平衡B移动;
A.正向移动 B.不移动 C.逆向移动 D.不一定.