题目内容
把铁和铜加入到氯化铁、氯化亚铁和氯化铜的混合溶液中,反应后铁有剩余则( )
| A、溶液中有Fe2+、Cu2+ |
| B、剩下的固体是Fe和Cu |
| C、溶液中有Fe3+、Fe2+ |
| D、剩下的固体是Fe,无Cu |
考点:铁的化学性质,铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:把金属铁和铜加入到氯化铁、氯化亚铁和氯化铜的混合溶液中,可能发生2Fe3++Fe=3Fe2+,Fe+Cu2+=Fe2++Cu,Cu+2Fe3+=2Fe2++Cu2+,以此解答该题.
解答:
解:把金属铁和铜加入到氯化铁、氯化亚铁和氯化铜的混合溶液中,可能发生2Fe3++Fe=3Fe2+,Fe+Cu2+=Fe2++Cu,Cu+2Fe3+=2Fe2++Cu2+,因铁剩余,则Fe3+、Cu2+完全反应,溶液中阳离子为Fe2+,剩下的固体是Fe和Cu.
故选B.
故选B.
点评:本题考查元素化合物知识,题目侧重于铁的性质的考查,难度不大,注意相关基础知识的积累,答题时注意铁过量的条件.

练习册系列答案
相关题目
制备相同质量的硝酸铜,从经济效益和环保角度考虑,最适宜采用的方法是( )
| A、Cu+HNO3(浓)→Cu(NO3)2 | |||||
| B、Cu+HNO3(稀)→Cu(NO3)2 | |||||
| C、Cu+AgNO3→Cu(NO3)2 | |||||
D、Cu
|
物质对应的用途(括号内是用途)错误的是( )
| A、单质硅(光导纤维) |
| B、钠钾合金(原子反应堆导热剂) |
| C、过氧化钠(潜水艇中供氧剂) |
| D、硫酸钡(医疗钡餐) |
下列说法不正确的是( )
| A、分子式为C3H8与C6H14的两种有机物一定互为同系物 |
| B、对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
| C、分子式C4H10表示的物质必是纯净物 |
D、有机物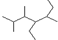 的名称:2,3,5-三甲基-4-乙基庚烷 的名称:2,3,5-三甲基-4-乙基庚烷 |
向含有Cu(NO3)2,Zn(NO3)2,Fe(NO3)3,AgNO3各0.1mol的混合溶液中加入0.1mol铁粉,充分搅拌反应后,下列结论错误的是( )
| A、溶液中析出0.05mol Cu |
| B、溶液中析出0.1mol Ag |
| C、溶液中Cu2+与Fe2+的浓度之比为1:2 |
| D、往反应后的溶液中再加入0.1mol 铁粉,铁粉恰好完全溶解 |
下列有关电解质溶液中微粒浓度关系正确的是( )
| A、pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
| B、含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C、0.1 mol/L NH4Cl与0.1 mol/L氨水等体积混合(pH>7):c(NH3?H2O)>c(NH4+)>c(Cl-)>c(OH-) |
| D、含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
下列说法错误的是( )
| A、硝酸的摩尔质量和6.02×1023个硝酸分子的质量(以克为单位)在数值上相等 |
| B、6.02×10个氮气分子和6.02×1023个氢气分子的质量比等于14:1 |
| C、32g氧气所含的原子数目约为2×6.02×1023 |
| D、通常情况下,近似值6.02×1023就是我们所说的阿伏伽德罗常数 |
 (1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组
(1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组