题目内容
11.下列物质属于非电解质的是( )| A. | 液氯 | B. | 淀粉 | C. | 硝酸钾 | D. | 液态氯化氢 |
分析 在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质,无论电解质还是非电解质,都一定为化合物,据此进行判断.
解答 解:A.液氯是单质,既不是电解质也不是非电解质,故A错误;
B.淀粉在水溶液和熔融状态下都不能导电,属于非电解质,故B正确;
C.硝酸钾在水溶液和熔融状态下都能够导电,是电解质,故C错误;
D.液态氯化氢,在溶液中能发生电离,溶液导电,是电解质,故D错误;
故选B.
点评 本题考查了电解质与非电解质的判断,题目难度不大,注意明确电解质与非电解质、强电解质与弱电解质的概念,特别注意:不是电解质的物质不一定属于非电解质.

练习册系列答案
相关题目
1.氨气是一种重要的化工产品,是生产铵盐、尿素等原料,工业合成氨的反应如下:
N2(g)+3H2(g)?2NH3(g)△H=一92.4KJ•mol-1
(1)已知H2(g)的燃烧热为285KJ/mol,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式.
(2)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将逆向(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为$\frac{a}{100V}$mol•L-1.(25℃时,NH3•H2O的电离平衡常数Kb≈2×10-5)
(3)工业上常通过如下反应合成尿素[CO(NH2)2]:
CO2(g)+2NH3(g)?CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3.反应中CO2( g)的物质的量随时间变化如表所示:
①20min时,υ正(CO2 )>80min时.υ逆(H2O)(填“>”、“=”或“<”).在t℃时,该反应额平衡常数表达式为K=$\frac{c({H}_{2}O)}{c(C{O}_{2}){c}^{2}(N{H}_{3})}$;
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO2和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大(填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为76.53(保留二位小数).
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变;则(t+10)℃下正确的图象可能是B(填图甲中的“A”或“B”).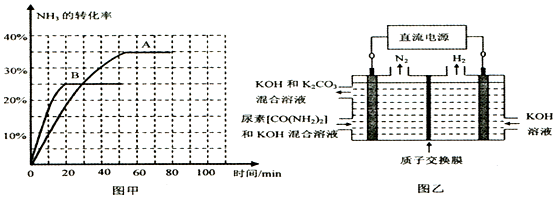
⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2-6e-+8OH-=CO32-+N2↑+6H2O,若两极共收集到气体22.4L(标况),则消耗的尿素为15g(忽略气体的溶解).
N2(g)+3H2(g)?2NH3(g)△H=一92.4KJ•mol-1
(1)已知H2(g)的燃烧热为285KJ/mol,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式.
(2)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将逆向(填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为$\frac{a}{100V}$mol•L-1.(25℃时,NH3•H2O的电离平衡常数Kb≈2×10-5)
(3)工业上常通过如下反应合成尿素[CO(NH2)2]:
CO2(g)+2NH3(g)?CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10molCO2和0.40molNH3.反应中CO2( g)的物质的量随时间变化如表所示:
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
②在100min时,保持其它条件不变,再向容器中充入0.050mo1CO2和0.20molNH3,重新建立平衡后CO2的转化率与原平衡相比将增大(填“增大”、“不变”或“减小”).
③上述可逆反应的平衡常数为76.53(保留二位小数).
④根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变;则(t+10)℃下正确的图象可能是B(填图甲中的“A”或“B”).

⑤图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素〔CO(NH2)2〕的碱性溶液制取氢气.该装置中阳极的电极反应式为CO(NH2)2-6e-+8OH-=CO32-+N2↑+6H2O,若两极共收集到气体22.4L(标况),则消耗的尿素为15g(忽略气体的溶解).
2.某学习小组探究Mg与NaHCO3溶液反应的机理,做了如下探究.
实验一:
(1)实验B的目的是与实验A做对照,排除水的干扰
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)
实验一:
| 实验A | 实验B | |
| 操作 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL饱和NaHCO3溶液. | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL蒸馏水. |
| 现象 | 有气体产生,20min后注射器内壁和底部产生大量白色沉淀 | 缓慢产生气体 |
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)
19.常温下,下列各组离子一定能在指定溶浓中大量共存的是( )
| A. | pH=l的溶液:Ba2+、Al3+、Cl-、SO42- | |
| B. | 能使酚酞试液变红的溶液:Na+、K+、HCO3-、I- | |
| C. | c(OH-)/c(H+)=10-12的溶液:NH4+、Cu2+、NO3-、Cl- | |
| D. | 含有0.1mol/LFe(NO3)2的溶液:H+、Mg2+、SCN-、SO42- |
6.向盛有不同试剂的试管b中分别滴加适量0.1mol/L FeCl3 溶液,下列对b中现象的解释正确的是( )
| 实验 | b中物质 | b中现象 | 结论或解释 | |
 | A | Mg(OH)2悬浊液 | 有红棕色胶体产生 | 发生反应:Fe3++3OH-═Fe(OH)3(胶体) |
| B | Cu粉 | 溶液变蓝,试管底部有固体 | 溶液变蓝的原因是:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C | 5%H2O2溶液 | 有气泡生成 | 该气体为氯气,双氧水强氧化性氧化Cl-产生 | |
| D | 饱和NaHCO3溶液 | 有气泡生成,且试管底部有固体 | 发生反应:Fe3++3HCO3-═Fe(OH)3+3CO2 |
| A. | A | B. | B | C. | C | D. | D |
16.下列有关铁、铜及其化合物的说法正确的是( )
| A. | 铁和铜在自然界中主要以游离态的形式存在 | |
| B. | 工业上在高温下用CO还原含Fe2O3的铁矿石炼铁 | |
| C. | 常温下铁与浓硫酸不反应 | |
| D. | 用激光照射硫酸铜溶液可观察到丁达尔现象 |
3.下列说法正确是( )
| A. | 符合分子通式CnH2n+2的烃一定都是烷烃,分子中均只含单键 | |
| B. | 通过石油裂化可以得到多种气态短链烃,其中包括重要化工原料 | |
| C. | 苯能使溴水褪色,说明苯环结构中含有碳碳双键 | |
| D. | 乙醇可以被氧气氧化成乙酸,但乙酸无法再被氧气氧化 |
20.分别进行如下表所示实验,现象和结论均正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 向FeBr2溶液中加入少量氯水,再加 CCl4振荡 | CCl4层无色 | Fe2+的还原性强于Br- |
| B | 向盐酸中滴入少量NaAlO2溶液 | 无明显现象 | AlO2-与H+未发生反应 |
| C | 向某溶液里滴加NaOH溶液并将湿润的红色石蕊试纸罝于试管口 | 试纸颜色无 明显变化 | 原溶液中无NH4+ |
| D | 常温下,测定等物质的量浓度的 Na2CO3和Na2SO3溶液的pH | 前者的pH 比后者的大 | 元素非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |
10.NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 将2mL 0.5mol•L-1Na2SiO3溶液滴入稀盐酸中制得H2SiO3胶体,所含胶粒数为0.001NA | |
| B. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| C. | 标准状况下,20g D2O分子中所含中子数为10NA | |
| D. | 将1mol Cl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA |