题目内容
6.在实验室配制100mL2.0mol/LH2SO4溶液:①用量筒量取98%,密度为1.84g•cm-3的浓硫酸10.9mL.
②将量取的98%浓硫酸沿烧杯内壁 加入盛有一定量蒸馏水的烧杯中,并搅拌 将其溶解,待冷却后,将溶液沿玻璃棒移入100mL的容量瓶中.
③用少量蒸馏水冲洗烧杯内壁2-3次,将冲洗液移入容量瓶,并轻轻摇动.
④向容量瓶内加水至刻度线1-2cm时,改用胶头滴管小心加水至溶液凹液面与刻度线相切,
⑤最后盖好瓶盖摇匀,将配好的溶液移入试剂瓶中并贴好标签.
分析 ①先求出浓硫酸的物质的量浓度,然后根据稀释定律C浓V浓=C稀V稀来计算;
②浓硫酸稀释放热,要将浓硫酸注入水中;待溶液冷却后,将溶液注入容量瓶,移液时用玻璃棒引流;容量瓶只有一条刻度线,故只能配制和其规格相对应的体积的溶液,据此选择;
③在配制溶液的过程中要防止硫酸的损失,故烧杯要洗涤2-3次,并据此分析洗涤液的处理;
④定容时,开始直接向容量瓶中倒水,后来改用胶头滴管逐滴注入;
⑤定容后要将溶液摇匀,容量瓶不能盛放溶液,据此分析.
解答 解:①98%,密度为1.84g•cm-3的浓硫酸的物质的量浓度c=$\frac{1000×1.84g/mL×98%}{98g/mol}$=18.4mol/L,设所需浓硫酸的体积为VmL,根据稀释定律C浓V浓=C稀V稀可知:18.4mol/L×VmL=2mol/L×100mL,解得V=10.9mL,故答案为:10.9;
②浓硫酸稀释放热,要将浓硫酸注入水中,方法是:将浓硫酸沿烧杯内壁注入烧杯中的水中,变倒边搅拌,待溶液冷却后,将溶液沿玻璃棒注入100mL容量瓶中,故答案为:沿烧杯内壁缓慢;烧杯;搅拌;冷却;玻璃棒;100;
③烧杯要洗涤2-3次,将洗涤液也注入容量瓶中,防止硫酸的损失,故答案为:2-3;容量瓶;
④定容是,要向容量瓶内加水至刻度线1-2cm时,改用胶头滴管小心加水至溶液凹液面与刻度线相切,故答案为:1-2cm;胶头滴管;
⑤定容后要将溶液摇匀,而容量瓶不能用于盛装溶液,故配制好溶液后要装瓶,故答案为:摇匀;试剂瓶.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和操作,属于基础型题目,难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
14.下列物质中互为同分异构体的是( )
| A. | 12C与14C | B. | CH3CH2OH与CH3COOH | ||
| C. | 甲烷与丙烷 | D. | CH3CH2CH2CH3与CH3CH(CH3)2 |
18.${\;}_{27}^{60}$CO是γ放射源,可用于农作物诱变育种,我国用该方法培育出了许多农作物新品种,对${\;}_{27}^{60}$CO原子的叙述不正确的是( )
| A. | 质量数是60 | B. | 质子数是60 | C. | 中子数是33 | D. | 电子数是27 |
15.如表是元素周期表一部分,列出了十种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是Ca(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),呈两性的氢氧化物是Al(OH)3(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键、共价键;
(4)用电子式表示元素③与⑧形成化合物的过程 .
.
(5)写出⑤与NaOH反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(6)写出工业冶炼⑤的化学方程式:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2第二步:Br2+SO2+2H2O=4H++SO42-+2Br-; 第三步Cl2+2Br-=2Cl-+Br2.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)在③~⑦元素中,原子半径最大的是Ca(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是HClO4(填物质化学式),呈两性的氢氧化物是Al(OH)3(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键、共价键;
(4)用电子式表示元素③与⑧形成化合物的过程
 .
.(5)写出⑤与NaOH反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(6)写出工业冶炼⑤的化学方程式:2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2第二步:Br2+SO2+2H2O=4H++SO42-+2Br-; 第三步Cl2+2Br-=2Cl-+Br2.
16.下列反应中,原子利用率最高的是( )
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | 乙烯的燃烧:CH2=CH2+3O2$\stackrel{点燃}{→}$ 2CO2+2H2O | |
| C. | Fe2O3+6HCl═2FeCl3+3H2O | |
| D. | Na2CO3+H2O+CO2═2NaHCO3 |
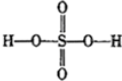 过硫酸:
过硫酸: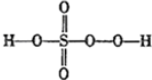
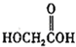 (b)
(b)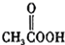 (c)H2O2(d)
(c)H2O2(d) (e)
(e) (f)
(f)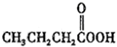 (g)O3(h)
(g)O3(h)