题目内容
6.室温下,下列各组离子在指定溶液中能大量共存的是( )| A. | 加入Al能放出H2的溶液中:NH4+,SO42-,Br-,NO3- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | 无色强酸性溶液中:Na+、Cl-、SO42-、Cu2+ | |
| D. | c(I-)=0.1 mol•L-1的溶液中:Na+、Fe2+、Cl-、SO42- |
分析 A.加入Al能放出H2的溶液中存在大量氢离子或氢氧根离子,铵根离子与氢氧根离子反应,硝酸根离子在酸性条件下与铝反应不会生成氢气;
B.铁离子能够氧化二氧化硫,硝酸根离子在酸性条件下能够氧化二氧化硫;
C.铜离子为有色离子;
D.c(I-)=0.1 mol•L-1的溶液中,四种离子之间不反应,都不与碘离子反应.
解答 解:A.加入Al能放出H2的溶液为酸性或碱性溶液,NH4+与氢氧根离子反应,NO3-在酸性溶液中具有强氧化性,与Al反应不会生成氢气,在溶液中一定不能大量共存,故A错误;
B.Fe3+和H+、NO3-都能够将SO2氧化成硫酸,Ba2+与硫酸反应生成硫酸钡沉淀,通入二氧化硫后不能大量共存,故B错误;
C.Cu2+为有色离子,在溶液中不能大量共存,故C错误;
D.Na+、Fe2+、Cl-、SO42-之间不发生反应,都不与I-反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
16.已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究温度对化学反应速率的影响,应选择①⑤或②④(填实验编号);
探究浓度对化学反应速率的影响,应选择①②或①③或④⑤(填实验编号);
若同时选择①②③溶液变浑浊的时间,探究比较改变不同反应物浓度对反应速率的影响对化学反应速率的影响.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
探究浓度对化学反应速率的影响,应选择①②或①③或④⑤(填实验编号);
若同时选择①②③溶液变浑浊的时间,探究比较改变不同反应物浓度对反应速率的影响对化学反应速率的影响.
17.对于4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g),试回答有关的问题:为了提高生成SO2的速率,可以采用的措施是( )
| A. | 增加FeS2的量 | B. | 增大O2的浓度 | C. | 升高温度 | D. | 减小压强 |
14.下列说法不正确的是( )
| A. | ⅠA元素的电负性从上到下逐渐减小,ⅦA元素的第一电离能从上到下逐渐减小 | |
| B. | 电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度 | |
| C. | NaH的存在能支持可将氢元素放在ⅦA的观点 | |
| D. | 氢原子中只有一个电子,故氢原子只有一个原子轨道 |
1.向Fe(NO3)2溶液中逐滴加入稀盐酸,溶液颜色变化应该是( )
| A. | 无变化 | B. | 颜色变浅 | C. | 变为棕黄色 | D. | 变为红褐色 |
11.有机物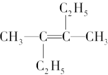 的命名正确的是( )
的命名正确的是( )
 的命名正确的是( )
的命名正确的是( )| A. | 2,3-二乙基-2-丁烯 | B. | 2,3-二乙基-3-丁烯 | ||
| C. | 3-甲基-2-乙基-2-戊烯 | D. | 3,4-二甲基-3-己烯 |
18.下表是五种短周期的原子半径及主要化合价.
已知铍的原子半径为0.089nm.
(1)用元素符号标出它们在周期表中对应位置(以下为周期表的一部分).
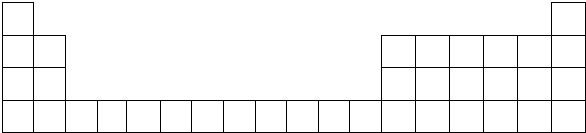
(2)B元素在元素周期表中的第三 周期IIIA 族;
(3)上述五种元素最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(4)A、D形成化合物的电子式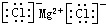 ;
;
(5)C、E形成化合物为SO2或SO3(填化学式),含化学键类型为共价键(填“离子键”或“共价键”).
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +7,-1 | -2 |
(1)用元素符号标出它们在周期表中对应位置(以下为周期表的一部分).

(2)B元素在元素周期表中的第三 周期IIIA 族;
(3)上述五种元素最高价氧化物对应水化物酸性最强的是HClO4(填化学式);
(4)A、D形成化合物的电子式
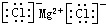 ;
;(5)C、E形成化合物为SO2或SO3(填化学式),含化学键类型为共价键(填“离子键”或“共价键”).
16.下列实验能获得成功的是( )
| A. | 用酸性高锰酸钾溶液鉴别乙烷和乙烯 | |
| B. | 用分液漏斗分离乙醛和水 | |
| C. | 用苯、溴水和铁粉混合制取溴苯 | |
| D. | 用紫色石蕊溶液检验苯酚弱酸性 |