题目内容
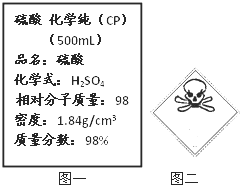
 如图,图一是硫酸试剂标签上的部分内容.下列说法正确的是
如图,图一是硫酸试剂标签上的部分内容.下列说法正确的是
- A.该硫酸的物质的量浓度为9.2 mol/L
- B.该浓硫酸中溶质、溶剂分子数目之比为9:1
- C.在盛放该药品的标签上应标出如图二所示的警示标记
- D.该硫酸与等质量的水混合所得溶液的物质的量浓度等于9.2 mol/L
B
分析:A、根据c=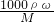 计算该硫酸的物质的量浓度.
计算该硫酸的物质的量浓度.
B、假定该浓硫酸为100g,则溶质硫酸为98g,溶剂水为2g,根据n= 计算溶质、溶剂的物质的量,据此计算判断.
计算溶质、溶剂的物质的量,据此计算判断.
C、浓硫酸具有腐蚀性,不是剧毒性品.
D、硫酸的浓度越大密度越大,该硫酸与等质量的水混合,质量变为2倍,密度降低,体积比原浓硫酸的2倍大,结合稀释定律判断.
解答:A、该浓硫酸的物质的量浓度c=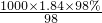 mol/L=18.4mol/L,故A错误;
mol/L=18.4mol/L,故A错误;
B、假定该浓硫酸为100g,则溶质硫酸为98g,n(H2SO4)=1mol,溶剂水为2g,n(H2O)= =
=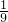 mol,所以n(H2SO4):n(H2O)=1mol:
mol,所以n(H2SO4):n(H2O)=1mol: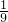 mol=9:1,所以该浓硫酸中溶质、溶剂分子数目之比为9:1,故B正确;
mol=9:1,所以该浓硫酸中溶质、溶剂分子数目之比为9:1,故B正确;
C、图中标志是剧毒品标志,浓硫酸具有腐蚀性,不是剧毒性品,故C错误;
D、硫酸的浓度越大密度越大,该硫酸与等质量的水混合,质量变为2倍,密度降低,体积比原浓硫酸的2倍大,根据稀释定律,稀释前后溶质硫酸的物质的量不变,所以浓度小于原浓硫酸的 ,混合所得溶液的物质的量浓度小于9.2 mol/L,故D错误.
,混合所得溶液的物质的量浓度小于9.2 mol/L,故D错误.
故选:B.
点评:本题考查物质的量浓度的计算、物质的量浓度与质量分数的关系等,难度中等,注意硫酸溶液的密度与浓度的关系,硫酸的浓度越大密度越大.
分析:A、根据c=
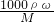 计算该硫酸的物质的量浓度.
计算该硫酸的物质的量浓度.B、假定该浓硫酸为100g,则溶质硫酸为98g,溶剂水为2g,根据n=
 计算溶质、溶剂的物质的量,据此计算判断.
计算溶质、溶剂的物质的量,据此计算判断.C、浓硫酸具有腐蚀性,不是剧毒性品.
D、硫酸的浓度越大密度越大,该硫酸与等质量的水混合,质量变为2倍,密度降低,体积比原浓硫酸的2倍大,结合稀释定律判断.
解答:A、该浓硫酸的物质的量浓度c=
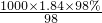 mol/L=18.4mol/L,故A错误;
mol/L=18.4mol/L,故A错误;B、假定该浓硫酸为100g,则溶质硫酸为98g,n(H2SO4)=1mol,溶剂水为2g,n(H2O)=
 =
=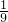 mol,所以n(H2SO4):n(H2O)=1mol:
mol,所以n(H2SO4):n(H2O)=1mol: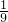 mol=9:1,所以该浓硫酸中溶质、溶剂分子数目之比为9:1,故B正确;
mol=9:1,所以该浓硫酸中溶质、溶剂分子数目之比为9:1,故B正确;C、图中标志是剧毒品标志,浓硫酸具有腐蚀性,不是剧毒性品,故C错误;
D、硫酸的浓度越大密度越大,该硫酸与等质量的水混合,质量变为2倍,密度降低,体积比原浓硫酸的2倍大,根据稀释定律,稀释前后溶质硫酸的物质的量不变,所以浓度小于原浓硫酸的
 ,混合所得溶液的物质的量浓度小于9.2 mol/L,故D错误.
,混合所得溶液的物质的量浓度小于9.2 mol/L,故D错误.故选:B.
点评:本题考查物质的量浓度的计算、物质的量浓度与质量分数的关系等,难度中等,注意硫酸溶液的密度与浓度的关系,硫酸的浓度越大密度越大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
下图图一是硫酸试剂标签上的部分内容。下列说法正确的是( )
| A.该硫酸的物质的量浓度为9.2 mol/L |
| B.该浓硫酸中溶质、溶剂分子数目之比为9:1 |
| C.在盛放该药品的标签上应标出如图二所示的警示标记 |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度等于9.2 mol/L |
 如图,图一是硫酸试剂标签上的部分内容.下列说法正确的是( )
如图,图一是硫酸试剂标签上的部分内容.下列说法正确的是( )