题目内容
2.一定量的CuS和Cu2S的混合物投入足量的HNO3中,共收集到气体VL(标准状况),向反应后的溶液中(Cu元素以Cu2+,S元素以SO42-形式存在)加入足量NaOH溶液,产生蓝色沉淀,过滤、洗涤、灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1:2.则V可能为( )| A. | 9.0L | B. | 11.2L | C. | 16.8L | D. | 22.4L |
分析 利用极限法解答,假设混合物全是CuS,或混合物全是Cu2S,根据n=$\frac{m}{M}$计算n(CuO),根据电子转移守恒计算n(CuS)、n(Cu2S),再根据电子转移数目守恒,计算n(NO)、n(NO2),根据V=nVm计算气体体积,实际气体介于二者之间.
解答 解:若混合物全是CuS,其物质的量n(CuS)=n(CuO)=$\frac{12g}{80g/mol}$=0.15mol,转移电子物质的量=0.15×(6+2)=1.2mol,NO和NO2的混合物,且体积比为1:2,设NO的物质的量为x、NO2的物质的量为2x,则3x+2x=1.2,解得x=0.24,故气体体积V=0.72mol×22.4L/mol=16.128L;
若混合物全是Cu2S,其物质的量n(Cu2S)=$\frac{1}{2}$n(CuO)=$\frac{1}{2}$×0.15mol=0.075mol,转移电子物质的量0.075×10=0.75mol,设NO为xmol、NO2为2xmol,3x+2x=0.75,计算得x=0.15,气体体积为:0.45mol×22.4L/mol=10.08L,
由于是CuS和Cu2S的混合物,则生成的气体体积介于10.08L~16.128L之间,故B正确,
故选B.
点评 本题考查氧化还原反应计算,题目难度中等,注意守恒思想与极限法的利用,是对学生综合能力的考查,有利于培养学生的分析、理解能力.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案
相关题目
2.下列依据相关实验得出的结论正确的是.( )
| A. | 向新制的氯水中加入NaHCO3粉末,有气泡产生,说明氯元素的非金属性强于碳 | |
| B. | 向Fe(NO3)3溶液中通入适量SO2气体后,再滴加BaCl2溶液,产生白色沉淀,说明Fe3+能够将H2SO3氧化为H2SO4 | |
| C. | 向NaOH溶液中滴加少量的MgCl2溶液,产生白色沉淀,然后再滴加足量的CuCl2溶液,沉淀变蓝色,说明 Ksp[Cu(OH)2]<Ksp[Mg(OH)2] | |
| D. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈紫色,说明该溶液一定含有钾元素 |
17.下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | B. | Na2CO3+H2SO4;Na2CO3+HCl | ||
| C. | CaCO3+H2SO4;CaCO3+HCl | D. | BaCl2+H2SO4;Ba(OH)2+H2SO4 |
7. 如图两个装置中,溶液体积均为200mL,开始时,电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol e-,若不考虑溶液体积的变化,则下列叙述正确的是( )
如图两个装置中,溶液体积均为200mL,开始时,电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol e-,若不考虑溶液体积的变化,则下列叙述正确的是( )
 如图两个装置中,溶液体积均为200mL,开始时,电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol e-,若不考虑溶液体积的变化,则下列叙述正确的是( )
如图两个装置中,溶液体积均为200mL,开始时,电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol e-,若不考虑溶液体积的变化,则下列叙述正确的是( )| A. | 在①中Cu棒为阳极;在②中Cu棒为负极 | |
| B. | 溶液的pH:①不变;②增大 | |
| C. | 电极上析出物质的质量:①<② | |
| D. | 电极反应式:①中阳极:4OH--4e-=2H2O+O2↑;②中正极:2H++2e-=H2↑ |
14.X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素.X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素.下列说法不正确的是( )
| Y | Z | M | |
| W |
| A. | 原子半径:W>Y>Z>M>X | |
| B. | N的一种氧化物可用作油漆和涂料 | |
| C. | 热稳定性:XM>X2Z | |
| D. | X2Z、WM4分子中各原子最外层均为8电子稳定结构 |
11.下列有机物的命名中,正确的是( )
| A. |  (2-乙基戊烷) (2-乙基戊烷) | B. |  (3-甲基-2-戊烯) (3-甲基-2-戊烯) | ||
| C. |  (2-甲基-戊炔) (2-甲基-戊炔) | D. |  (1-甲基-5-乙基苯) (1-甲基-5-乙基苯) |
12.化学是一门实用性很强的科学,与社会、环境等密切相关.下列说法错误的是( )
| A. | “静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 | |
| B. | 维生素C具有较强还原性,高温烹饪蔬菜会导致维生素C损失 | |
| C. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| D. | 在食品包装袋中放入生石灰,可防止食物被氧化变质 |
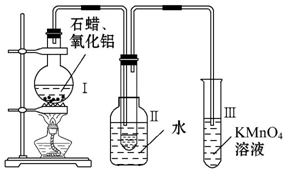 某研究性学习小组在实验室中模拟石油的催化裂化,装置如图,实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实验后闻试管Ⅱ中液体气味,具有汽油的气味.
某研究性学习小组在实验室中模拟石油的催化裂化,装置如图,实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实验后闻试管Ⅱ中液体气味,具有汽油的气味.