题目内容
5.下列对浓硫酸的叙述中正确的是( )| A. | 将1〜2滴浓硫酸滴入紫色石蕊试液中,溶液先变红后变黑 | |
| B. | 浓硫酸因为具有吸水性,所以可以使蔗糖炭化 | |
| C. | 浓硫酸和Na2SO3反应制取SO2时,浓硫酸表现出强氧化性 | |
| D. | 浓硫酸和铜片在加热条件下反应时,浓硫酸既表现出酸性,又表现出强氧化性 |
分析 A、将1〜2滴浓硫酸滴入紫色石蕊试液中,溶液只变红;
B、蔗糖炭化是浓硫酸的脱水性;
C、浓硫酸和Na2SO3反应制取SO2时,不挥发性酸制挥发性酸;
D、金属与浓硫酸反应体现浓硫酸的酸性和强氧化性.
解答 解:A、将1〜2滴浓硫酸滴入紫色石蕊试液中,溶液只变红,而不变黑,故A错误;
B、蔗糖炭化是浓硫酸的脱水性,而不是吸水性,故B错误;
C、浓硫酸和Na2SO3反应制取SO2时,不挥发性酸制挥发性酸,非氧化还原反应,故C错误;
D、金属与浓硫酸反应体现浓硫酸的酸性和强氧化性,与铜反应生成二氧化硫体现氧化性,生成硫酸铜体现酸性,故D正确;
故选D.
点评 本题考查浓硫酸的性质,为高频考点,综合考查元素化合物知识,把握发生的反应为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.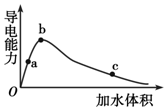 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离程度:a<b<c | |
| B. | 溶液的pH值:b>a>c | |
| C. | 蘸取c点溶液滴在湿润的pH试纸上,测得pH值一定偏大 | |
| D. | 若分别向a、b、c三点的溶液中,加入同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c |
16.紫外线作用下氧气可生成臭氧:3O2(g)?2O3(g),一定条件下反应达到平衡状态的标志是( )
| A. | 单位时间内生成2 mol O3,同时消耗3 mol O2 | |
| B. | O2的消耗速率0.3 mol•L-1•s-1,O3的消耗速率0.2 mol•L-1•s-1 | |
| C. | 容器内,2种气体O3、O2浓度相等 | |
| D. | 恒容时,密度不再发生变化,气体的平均相对分子质量也不再发生变化 |
13.室温下,0.1mol/LNa2CO3溶液加适量水稀释,下列各项随着加水量的增大而减小的是( )
| A. | n(OH-) | B. | 溶液的pH | ||
| C. | n(H+)•c(OH-) | D. | $\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$ |
20.常温下,下列物质不能与稀盐酸反应的是( )
| A. | Al | B. | MnO2 | C. | Al(OH)3 | D. | NaHCO3 |
10.对于反应:S(g)+Cl2(g)?SCl2 (g)△H<0,下列措施中能增大正反应速率且平衡常数不变的是( )
| A. | 通入大量的Cl2 | B. | 增大容器容积 | C. | 移去部分SCl2 | D. | 升高温度 |
17.下列有关“物质→类别”的对应关系正确的是( )
| A. | 纯碱→碱 | B. | 氧化铁→碱性氧化物 | ||
| C. | 次氯酸→强酸 | D. | 氢氧化铁胶体→纯净物 |
13.往下列各组物质的混合溶液中分别通入适量CO2,看不到明显现象的是( )
| A. | Na2SiO3和饱和Na2CO3溶液 | B. | CaCl2溶液和NaOH | ||
| C. | Ba(NO3)2和CaCl2 | D. | NaAlO2和Ca(ClO)2 |
14. “长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
 “长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼 (C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A. | 从a口通入四氧化二氮气体 | |
| B. | 从d口排除的是NO气体 | |
| C. | H+由A流向B | |
| D. | A极发生的电极反应式:C2H8N2-16e-+8H2O=CO2+N2+16H+ |