题目内容
15. 一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO(g)+H2O (g)═CO2(g) 十 H2 (g);△H<0
(1)在850℃时,CO和H2O浓度变化如图,则 0~4min的平均反应速率v(CO2)=0.03mol•L-1•min-1
(2)t1℃时,在相同容器中发生上述反应,各物质的浓度变化如表:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
(3)t2℃时,化学反应CO (g)+H2O (g)?CO2(g)+H2 (g)的平衡浓度符合c(CO2)•c(H2)═2c(CO)•c(H2O),则t2℃<850℃,判断依据是:t2℃的平衡常数为2,大于850℃的平衡常数1,平衡右移
(4)在t1℃达平衡时,又充入CO,再次平衡时,混合气体中H2O的体积分数将减小(填“增大”、“减小”或“无法确定”) H2O的转化率将增大(填“增大”、“减小”或“无法确定”)
(5))判断该反应达到化学平衡状态的依据是AB(填序号):
A.V(正)(CO)=V (逆)(CO2)
B.CO消耗速率等于H2的消耗速率
C. 容器内压强保持不变
D.混合气体的密度保持不变
E.容器中气体的平均相对分子质量不随时间而变化
F.混合气体的质量保持不变.
分析 (1)根据v=$\frac{△c}{t}$求得CO的速率,再利用速率之比等于计量数之比,求得二氧化碳的速率;
(2)①根据平衡常数的定义求得;
②根据图中数据可知,在5min~6min间,CO减小了0.02mol/L,水增加了0.05mol/L,CO2增加了0.02mol/L,由此可以看出,CO减小的浓度等于CO2增加的浓度,反应正向移动,它们变化的浓度也符合反应中的计量数的关系,所以可以看出在第5分钟时改变的条件是增加了水的浓度,据此答题;
(3)比较两个温度下的平衡常数的大小可以判断出温度的高低;
(4)在t1℃达平衡时,又充入CO,平衡正向移动,所以混合气体中H2O的体积分数将减小,H2O的转化率将增大;
(5))A.V(正)(CO)=V(正)(CO2)=V (逆)(CO2),达平衡状态;
B.CO消耗速率等效于H2的生成速率等于H2的消耗速率,达平衡状态;
C. 容器内压强一直保持不变;
D.混合气体的密度一直保持不变;
E.容器中气体的平均相对分子质量一直不随时间而变化;
F.混合气体的质量一直保持不变.
解答 解:(1)根据v=$\frac{△c}{t}$求得CO的速率为$\frac{0.2-0.08}{4}$mol•L-1•min-1=0.03mol•L-1•min-1,在反应中一氧化碳与二氧化碳计量数之比为1:1,根据速率之比等于计量数之比,可知二氧化碳的速率也为0.03mol•L-1•min-1,故答案为:0.03mol•L-1•min-1;
(2)①根据题目表格中的数据可知,当在3min时各组成成分的浓度不再变化,此时反应处于平衡状态,根据平衡常数的定义可知K=$\frac{0.1×0.1}{0.2×0.1}$=0.5,
故答案为:0.5;
②根据图中数据可知,在5min~6min间,CO减小了0.02mol/L,水增加了0.05mol/L,CO2增加了0.02mol/L,由此可以看出,CO减小的浓度等于CO2增加的浓度,反应正向移动,它们变化的浓度也符合反应中的计量数的关系,所以可以看出在第5分钟时改变的条件是增加了水的浓度,其增加的浓度为0.05mol/L+0.02mol/L=0.07mol/L,所以水的浓度增加到0.286mol/L,故答案为:向右;将H2O (g)浓度增加到0.286 mol•L-1;
(3)由于c(CO2)•c(H2)=2c(CO)•c(H2O),根据平衡常数的定义可知,在t2℃时,K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$=2,大于850℃的平衡常数1,平衡右移,而该反应为放热反应,所以温度要低于850℃,故答案为:<; t2℃的平衡常数为2,大于850℃的平衡常数1,平衡右移;
(4)在t1℃达平衡时,又充入CO,平衡正向移动,所以混合气体中H2O的体积分数将减小,H2O的转化率将增大,故答案为:减小;增大;
(5))A.V(正)(CO)=V(正)(CO2)=V (逆)(CO2),达平衡状态,故正确;
B.CO消耗速率等效于H2的生成速率等于H2的消耗速率,达平衡状态,故正确;
C. 容器内压强一直保持不变,故错误;
D.混合气体的密度一直保持不变,故错误;
E.容器中气体的平均相对分子质量一直不随时间而变化,故错误;
F.混合气体的质量一直保持不变,故错误;故选AB.
点评 本题主要考查了反应速率的计算、平衡常数的计算、影响平衡移动的因素及平衡常数的应用,中等难度,解题的易错点在于第(3)小问,平衡常数的应用.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案| A. | 碳酸钠可以用于治疗胃酸过多 | |
| B. | 过氧化钠可做航天员的供氧剂 | |
| C. | 金属钠有强还原性,能和硫酸铜溶液反应,但不能析出金属铜 | |
| D. | 为使面包松软可口可用碳酸氢钠做发泡剂 |
| A. | Na2CO3→NaOH | B. | BaCl2→Ba(OH)2 | C. | FeCl3→Fe(OH)3 | D. | CaCO3→CaCl2 |
| A. | 低温、低压 | B. | 低温、高压 | C. | 高温、高压 | D. | 高温、低压 |
| A. | Na+ | B. | Al3+ | C. | Fe3+ | D. | Fe2+ |
| A. | 保持温度和容器内压强不变,充入1molNH3(g) | |
| B. | 保持温度和容器内压强不变,充入1molAr(g) | |
| C. | 保持温度和容器体积不变,充入1molN2(g) | |
| D. | 保持温度和容器体积不变,充入1molNH3(g) |
| A. | 由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 | |
| B. | 增大压强可加快SO2转化为SO3的速率 | |
| C. | 黄绿色的氯水光照后颜色变浅 | |
| D. | 在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
| A. | FeS2作还原剂,铁元素被还原 | |
| B. | Fe2O3和SO2都既是氧化产物又是还原产物 | |
| C. | 每生成1 mol Fe2O3,有4mol硫被氧化 | |
| D. | 每1 mol硫被氧化,转移电子5.5mol |
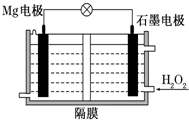 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )| A. | Mg电极是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的pH增大 | D. | 电子从石墨电极移向Mg电极 |