题目内容
19.金属铜能被氯化铁浓溶液腐蚀,其化学反应是:Cu+2FeCl3═CuCl2+2FeCl2.现将有铜的印刷线路板浸入120mL氯化铁浓溶液中,有9.6g铜被腐蚀掉.取出印刷线路板,向溶液中加入8.4g铁粉,经充分反应,溶液中还存在4.8g不溶解的物质.(设溶液体积不变,且不考虑金属离子水解).请回答下列问题:(1)向溶液中加入铁粉后,发生反应的离子反应方程式为Fe+2Fe3+═3Fe2+,Fe+Cu2+═Fe2++Cu.
(2)充分反应后,溶液中存在4.8g不溶物的成分为Cu.
(3)充分反应后溶液中一定不存在的金属离子为Fe3+.
(4)比较Fe2+、Fe3+、Cu2+的氧化性大小:Fe3+>Cu2+>Fe2+.
(5)试计算最后溶液中Fe2+离子的物质的量浓度5.0mol/L.
分析 (1)依据反应:Cu+2FeCl3═CuCl2+2FeCl2、Fe+CuCl2=FeCl2+Cu判断溶液中剩余的金属离子、固体物质的成分;
(2)依据Cu+2FeCl3═CuCl2+2FeCl2计算即可;
(3)反应顺序是Fe先和过量的Fe3+反应,再置换部分Cu2+,据此回答判断;
(4)氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,据此回答;
(5)利用物质的量守恒以及电子得失守恒计算即可.
解答 解:(1)向氯化铁、氯化铜溶液中加入铁粉后,发生反应的离子反应方程式为:Fe+2Fe3+═3Fe2+,Fe+Cu2+═Fe2++Cu;
故答案为:Fe+2Fe3+═3Fe2+;Fe+Cu2+═Fe2++Cu;
(2)加入Fe粉前,溶液中有Cu2+,Fe2+,Cl-,可能还有Fe3+,8.4gFe为0.15mol,9.6gCu为0.15mol,若无Fe3+,那么Fe恰好把9.6gCu全部置换,现在只有4.8g不溶物,所以不可能为Fe,只能是Cu,故答案为:Cu;
(3)反应顺序是Fe先和过量的Fe3+反应,再置换部分Cu2+,溶液中一定不存在的金属离子为Fe3+,存在Cl-、Fe2+、Cu2+,故答案为:Fe3+;
(4)由化学方程式Cu+2FeCl3=CuCl2+2FeCl2,氧化剂的氧化性强于氧化产物的氧化性,即溶液中离子氧化性Fe3+大于Cu2+,根据金属活动顺序表,Cu2+>Fe2+,所以氧化性顺序是:Fe3+>Cu2+>Fe2+,
故答案为:Fe3+>Cu2+>Fe2+;
(5)加入Fe,反应顺序是Fe先和过量的Fe3+反应,再置换部分Cu2+,所以存在Cl-,Fe2+,Cu2+;溶液中剩余的Cu元素为9.6-4.8=4.8g,0.075mol,综合来看,溶液中是4.8gCu和8.4gFe恰好完全还原了Fe3+,Cu失电子为0.15mol,Fe失电子0.3mol,合计0.45mol,所以原有Fe3+0.45mol,最后所有的Fe元素都变成Fe2+,故[Fe2+]=$\frac{0.15+0.45}{0.12}$mol/L=5.0mol/L,
故答案为:5.0.
点评 本题主要考查的是铜以及铁之间的转化关系、计算,属于中等题,锻炼了同学们分析问题、解决问题的能力,难度中等.

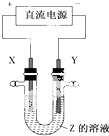 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 外加电流的阴极保护法中,Y是待保护金属 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 电镀工业中,X是待镀金属,Y是镀层金属 | |
| D. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 |
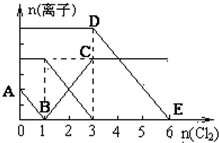 已知:2Fe3++2I-═2Fe2++I2,向1L含有Fe2+、I━、Br━的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )
已知:2Fe3++2I-═2Fe2++I2,向1L含有Fe2+、I━、Br━的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )| A. | 线段BC代表Fe3+物质的量的变化情况 | |
| B. | 原混合溶液中c(FeBr2)=6 mol/L | |
| C. | 原溶液中n (Fe2+):n (I-):n(Br-)=2:1:3 | |
| D. | 当通入Cl22mol时,溶液中已发生的反应可表示为2Fe2++2I━+2Cl2═2Fe3++I2+4Cl━ |
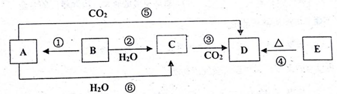
(1)反应⑤可用于潜水艇中制取氧气,相关的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,氧化剂是Na2O2,还原剂是Na2O2;
(2)根据反应②相关的现象,从表格下方找出相应性质序号填在表格中,并在对应的位置写上该反应的化学方程式.
| 现象 | 单质B的相关性质(填序号) | 相关的化学方程式 | |
| Ⅰ | 单质B浮在水面上 | ||
| Ⅱ | 熔成一个小球 | ||
| Ⅲ | 四处游动,发出嘶嘶的声音 | ||
| Ⅳ | 滴入酚酞试剂,溶液变红 |
(3)D和E分别与等浓度的盐酸反应,相同条件下生成等体积的气体,则以下说法正确的是:①③(填序号)①消耗D的质量较多;②消耗E的质量较多;③D消耗盐酸的体积更大 ④E消耗盐酸的体积更大.
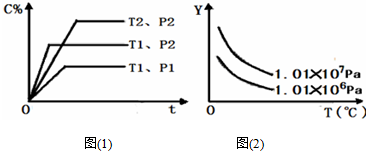
| A. | 反应物A的百分含量 | B. | 反应物B的平衡转化率 | ||
| C. | 平衡混合气的密度 | D. | 平衡混合气的总物质的量 |
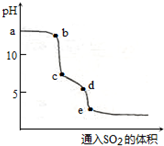 PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx.
PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx.