题目内容
10.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )| A. | Y既可是金属也可是非金属 | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | X、Z形成的某化合物在熔融状态下不导电 | |
| D. | WY2分子中既有非极性键又有极性键 |
分析 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,则W为C,X为Al,Z原子比X原子的核外电子数多4,Z为Cl,Y的原子序数在13~17之间,Y可能为Si、P、S,以此来解答.
解答 解:短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,则W为C,X为Al,Z原子比X原子的核外电子数多4,Z为Cl,Y的原子序数在13~17之间,Y可能为Si、P、S,
A.Y只能为非金属元素,故A错误;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则W、X、Y、Z的原子半径大小顺序可能是X>Y>Z>W,故B错误;
C.X、Z形成的某化合物为氯化铝,为共价化合物,在熔融状态下不导电,故C正确;
D.WY2分子可为CS2分子,分子中只含极性共价键,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子结构推断元素为解答的关键,侧重分析与推断能力的考查,注意周期律及元素化合物知识的应用,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.室温下如图,关闭活塞,在左右两室(体积相同)各充入一定量H2和Cl2,且恰好使两容器内气体密度相同,打开活塞,点燃使H2与Cl2充分反应生成氯化氢气体:H2+Cl2=2HCl,恢复到原温度后,下列判断正确的是( )

| A. | 开始时左右两室分子数相同 | B. | 最终容器内无H2存在 | ||
| C. | 反应前后H2室压强相同 | D. | 最终容器内密度与原来相同 |
18.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:K+、NH4+、SO42-、NO3- | |
| B. | 0.1 mol/L NaAlO2溶液:Fe3+、H+、Cl-、SO42- | |
| C. | 与铝反应产生大量气体的溶液:Na+、K+、CO32-、NO3- | |
| D. | 使甲基橙试液显黄色的溶液:Fe2+、Mg2+、NO3-、Cl- |
15.分类是学习和研宄化学的一种常用的科学方法,下列分类合理的是( )
①根据酸分子中含有H原子个数将酸分为一元酸、二元酸等
②碱性氧化物一定是金属氧化物
③根椐丁达尔现象可将分散系分为胶体、溶液和浊液
④SiO2能与NaOH溶液反应生成Na2SiO3和水,SiO2是酸性氧化物.
①根据酸分子中含有H原子个数将酸分为一元酸、二元酸等
②碱性氧化物一定是金属氧化物
③根椐丁达尔现象可将分散系分为胶体、溶液和浊液
④SiO2能与NaOH溶液反应生成Na2SiO3和水,SiO2是酸性氧化物.
| A. | ②③ | B. | ②④ | C. | ①②④ | D. | ②③④ |
2.电解100mL含c(H+)=0.3mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是( )
| A. | 0.10mol∕L Ag+ | B. | 0.20mol∕L Cu2+ | C. | 0.20mol∕L Zn2+ | D. | 0.20mol∕LPb2+ |
20.下列各组离子一定能大量共存的是( )
| A. | 含有大量Ba2+的溶液:Cl- K+ SO42- CO32- | |
| B. | 含有大量H+的溶液:Mg2+ Na+ SO42- CO32- | |
| C. | 含有大量 OH-的溶液:Cu2+ NO3- SO42- CO32- | |
| D. | 含有大量Na+的溶液:H+ K+ SO42- NO3- |
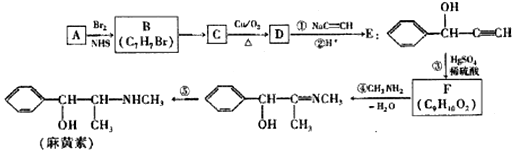
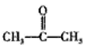
 ,E中含氧官能团的名称为羟基.
,E中含氧官能团的名称为羟基. .
. +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. (任写一种).
(任写一种).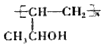 )的合成路线,其它试剂及溶剂任选.
)的合成路线,其它试剂及溶剂任选.