题目内容
工业上用CO来生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。图1表示反应过程中能量的变化情况;图2表示一定温度下,向固定体积为2 L的容器中加入4 mol H2和一定量的CO后,CO(g)和CH3OH(g)的物质的量
CH3OH(g)。图1表示反应过程中能量的变化情况;图2表示一定温度下,向固定体积为2 L的容器中加入4 mol H2和一定量的CO后,CO(g)和CH3OH(g)的物质的量


请回答下列问题:
(1)在图1中,曲线________(填“a”或“b”)表示反应使用了催化剂;该反应属于________(填“吸热”或“放热”)反应。
(2)根据图2判断下列说法中正确的是________(填序号)。ks5u
a.起始充入的CO的物质的量为2 mol b.增大CO的浓度,CO的转化率增大
c.容器中压强恒定时,说明反应已达平衡状态
d.保持温度和密闭容器的容积不变,再充入1 mol CO和2 mol H2,再次达到平衡时,n(CH3OH)/n(CO)的值会变小。
(3)从反应开始至达到平衡,v(H2)=________。该温度下CO(g)+2H2(g) ![]() CH3OH(g)的化学平衡常数为________;若保持其他条件不变,将反应体系升温,则该反应的化学平衡常数将________(填“增大”“减小”或“不变”)。
CH3OH(g)的化学平衡常数为________;若保持其他条件不变,将反应体系升温,则该反应的化学平衡常数将________(填“增大”“减小”或“不变”)。
(4)已知CH3OH(g)+![]() O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ·mol-1,H2O(l)===H2O(g) ΔH=+44 kJ·mol-1,请写出32 g CH3OH(g)完全燃烧生成CO2和液态水的热化学方程式:___________________。
O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ·mol-1,H2O(l)===H2O(g) ΔH=+44 kJ·mol-1,请写出32 g CH3OH(g)完全燃烧生成CO2和液态水的热化学方程式:___________________。
(1)b 放热 (2)ac
(3)0.15 mol·L-1·min-1 12 减小 ks5u
(4)CH3OH(g)+![]() O2(g)===CO2(g)+2H2O(l) ΔH=-280.9 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=-280.9 kJ·mol-1

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案近年来,碳和碳的化合物在生产生活实际中应用广泛。
(1)在2升的密闭容器中,充有2mol CO与4mol 水蒸气,在催化剂作用下进行如下化学反应:CO(g)+H2O(g) CO2(g)+H2(g),CO的转化率和温度t的关系如下表:
CO2(g)+H2(g),CO的转化率和温度t的关系如下表:
|
t(℃) |
750 |
850 |
1000 |
|
CO% |
0.7 |
2/3 |
0.5 |
1000℃时该反应的平衡常数为___________________。850℃时,向该容器中重新通入1mol CO、1.5mol H2O、0.5mol CO2和2molH2,此时反应___________(填“向右进行”、“向左进行”或“处于平衡状态”)。
(2)已知:C(s)+O2 (g) ===CO2(g) △H1=﹣393.5kJ·mol-1
2H2(g)+O2(g)=== 2H2O(g) △H2=﹣483.6kJ·mol-1
C(s)+H2O(g)=== CO(g)+H2(g) △H3=+131.3kJ·mol-1
则CO和H2O生成CO2和H2的热化学方程式为_______________________________。
(3) 目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。现向体积为1 L的密闭容器中,充入
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。现向体积为1 L的密闭容器中,充入
1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=_____________;
②若改变条件使平衡向正反应方向移动,则平衡常数______________(填序号)
a.可能不变 b.可能减小 c.可能增大 d.不变、减小、增大皆有可能
(4)NaHCO3的水溶液呈碱性,其原因是(用文字叙述)_______________________。常温下,向100mL
0.2mol/LNaHCO3溶液中滴加amol/L的醋酸溶液,当滴加到溶液呈中性时,所用去的醋酸体积刚好也
为100mL,此时醋酸的电离常数为b, 用含b的代数式表示醋酸的浓度a=_____________________。
(1)目前工业上利用CO2来生产燃料甲醇,可将CO2变废为宝.已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
则反应2CO2(g)+4H2O(g)═2CH3OH(l)+3O2(g)△H=______kJ?mol-1
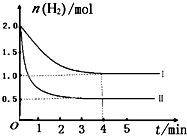
(2)T℃时,已知反应:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0.在T℃下,将2mol CO2和2mol H2充入1L的密闭容器中,测得H2的物质的量随时间的变化情况如图中曲线I所示.
①按曲线I计算反应从0到4min时,υ(H2)=______.
②在T℃时,若仅改变某一外界条件时,测得H2的物质的量随时间的变化情况如图中曲线Ⅱ所示,则改变的外界条件为______.计算该反应按曲线II进行,达到平衡时,容器中c(CO2)=______.
(3)已知25℃时,乙酸和碳酸的电离平衡常数如下表:
| 物质的化学式 | CH3COOH | H2CO3 | |
| 电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 | K2=5.6×10-11 |
②在25℃时,在乙酸溶液中加入一定量的NaHCO3,保持温度不变,所得混合液的pH=6,那么混合液中
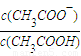 =______.
=______.③向0.1mol?L -1CH3COOH溶液中加入少量CH3COONa晶体,保持温度不变,下列有关说法正确的是______(填代号).
a.溶液的pH增大 b.CH3COOH的电离程度增大
c.溶液的导电能力减弱 d.溶液中c(OH-)?c(H+)不变.

 (2013?临沂三模)工业上“固定”和利用CO2能有效地减轻“温室效应”.
(2013?临沂三模)工业上“固定”和利用CO2能有效地减轻“温室效应”.