题目内容
15.M、Q、R、V为分别占有前3周期的元素,其原子序数依次增加,M和R、Q和V属于同一主族,且它们的最外层电子数之和为14,下列说法中正确的是( )| A. | 单质的沸点:M>Q | |
| B. | Q元素的阴离子和V元素的阴离子都只有还原性 | |
| C. | Q与R可以组成2种离子化合物 | |
| D. | M、Q、R、V四种元素组成的化合物的水溶液可以是碱性、中性和酸性 |
分析 M、Q、R、V为分别占有前3周期的元素,原子序数依次增加,则M一定在第一周期,V一定位于第三周期,又M和R、Q和V属于同一主族,则Q、R一定都位于第二周期,则M为H,R为Na,Q和V属于同一主族,四种元素最外层电子数之和为14,则Q和V最外层电子数为:$\frac{14-1-1}{2}$=6,故Q为O元素,V为S元素,结合元素周期律与物质性质解答.
解答 解:M、Q、R、V为分别占有前3周期的元素,原子序数依次增加,则M一定在第一周期,V一定位于第三周期,又M和R、Q和V属于同一主族,则Q、R一定都位于第二周期,则M为H,R为Na,Q和V属于同一主族,四种元素最外层电子数之和为14,则Q和V最外层电子数为:$\frac{14-1-1}{2}$=6,故Q为O元素,V为S元素,
A.H2和O2均为分子晶体,相对分子质量H2<O2,则沸点H2<O2,故A错误;
B.Q元素的阴离子和V元素的阴离子分别为O2-或O22-、S2-,O22-有还原性也有氧化性,故B错误;
C.Na和O可以组成Na2O和Na2O2两种离子化合物,故C正确;
D.M、Q、R、V四种元素形成的化合物为NaHSO3或NaHSO4,其水溶液均是酸性,故D错误;
故选C.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,利用提供数据及位置关系推断元素是解题的关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
5.在下列给定条件下的溶液中,一定能大量共存的离子组是( )
| A. | 无色溶液:Cu2+、H+、Cl-、HSO3- | |
| B. | 能使pH试纸呈红色的溶液:Fe2+、Na+、Cl-、NO3- | |
| C. | Na2CO3溶液:K+、NO3-、Cl-、Al3+ | |
| D. | $\frac{{K}_{W}}{c(H)}$=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- |
6.下列有关化学与生活、技术的说法中不正确的是( )
| A. | 考古时可用12C测定一些文物的年代 | |
| B. | 可在元素周期表的过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 乙烯是一种重要的基本化工原料,它的产量可以用来衡量一个国家的石油化工发展水平 | |
| D. | 红葡萄酒的密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯 |
3.下列关于氧化物的叙述中,正确的是( )
| A. | 酸性氧化物都可以与强碱溶液反应 | |
| B. | 与水反应生成酸的氧化物都是酸性氧化物 | |
| C. | 金属氧化物都是碱性氧化物或两性氧化物 | |
| D. | 不能与酸反应的氧化物一定能与碱反应 |
10.由A、B、C、D四种金属按表中装置进行实验.
根据实验现象回答下列问题:
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
| 装置 | 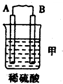 | 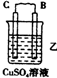 |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置乙中正极的电极反应式是Cu2++2e-═Cu.
②四种金属活动性由强到弱的顺序是D>A>B>C.
20.某溶液中有NH4+、Mg2+、Fe2+和Al3+四种阳离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子组合是( )
| A. | NH4+、Mg2+ | B. | Mg2+、Fe2+ | C. | NH4+、Fe2+ | D. | Mg2+、Al3+ |
7.某烃甲与氢气反应后的产物乙为(CH3)2CHCH2CH3,则相关说法不合理的是( )
| A. | 产物乙的系统命名为2-甲基丁烷 | |
| B. | 烃甲可能是2-甲基-1,3-丁二烯 | |
| C. | 0.1 mol产物乙完全燃烧可消耗17.92L O2 | |
| D. | 烃甲与乙炔可能是同系物 |
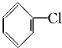 制取
制取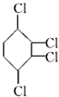 ,其合成流程如下:
,其合成流程如下:
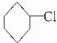 .
. ,
,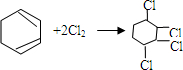 .
.