题目内容
19.设NA为阿伏伽德罗常数的值,下列说法不正确的是( )| A. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| B. | 2.8gN2和CO的混合气体中所含质子数为1.4NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA | |
| D. | 50mL12mol/L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
分析 A、H218O与D2O的摩尔质量均为20g/mol,且均含10个中子;
B、氮气和CO的摩尔质量均为28g/mol,且两者均含14个质子;
C、过氧化钠和水的反应中,氧元素的价态由-1价变为0价;
D、二氧化锰在加热的条件下只能与浓盐酸反应,和稀盐酸不反应.
解答 解:A、H218O与D2O的摩尔质量均为20g/mol,故2.0g混合物的物质的量为0.1mol,且均含10个中子,故0.1mol混合物中含NA个中子,故A正确;
B、氮气和CO的摩尔质量均为28g/mol,故2.8g混合物的物质的量为0.1mol,且两者均含14个质子,故0.1mol混合物中含1.4NA个质子,故B正确;
C、过氧化钠和水的反应中,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时,转移0.2NA个电子,故C正确;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应,随反应的进行盐酸浓度变小,当是稀盐酸反应就停止了,故转移的电子数小于0.3NA个,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
9.胶体与溶液的本质区别是( )
| A. | 是否属于混合物 | B. | 是否无色透明 | ||
| C. | 分散质粒子直径大小 | D. | 有无丁达尔效应 |
10.下列说法错误的是( )
| A. | 糖类、油脂和蛋白质均是高分子化合物 | |
| B. | 雾能产生丁达尔效应,雾属于胶体 | |
| C. | 新制氯水、HClO和SO2都有漂白作用 | |
| D. | 硝酸能与苯发生取代反应 |
7.下列溶液的物质的量浓度不是1mol/L的是( )
| A. | 1L溶液中含1 mol硫酸根离子的H2SO4溶液 | |
| B. | 将500克胆矾溶于2升水中 | |
| C. | 200mL溶液中含32克硫酸铜的溶液 | |
| D. | 把125克胆矾溶于水,配成500mL溶液 |
11.某原电池装置如右图所示,下列说法正确的是( )
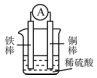

| A. | 铜棒逐渐溶解,溶液由无色慢慢地变为黄色 | |
| B. | 铁棒为负极,电子从铁棒经外电路流向铜棒 | |
| C. | 电池工作一段时间后,溶液的酸性将增强 | |
| D. | 该电池的总反应为Fe2++Cu═Fe+Cu2+ |
8.下列反应的离子反应方程式正确的是( )
| A. | 过量的二氧化碳通入NaOH溶液中:CO2+OH-═HCO3- | |
| B. | 氯气通入水中:Cl2+H2O═Cl-+ClO-+2H+ | |
| C. | 硫酸亚铁溶液加入过氧化氢溶液 Fe2++2H2O2+4H+═Fe3++4H2O | |
| D. | 向AlCl3溶液中过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
2.亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,物理性质与NaCl极为相似.相关化学性质如图所示,下列说法不正确的是( )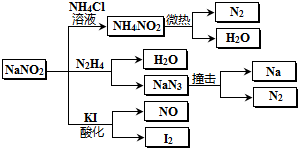

| A. | 分解NaN3盐每产生1molN2 转移6mol e- | |
| B. | NaNO2与N2H4反应中,NaNO2是氧化剂 | |
| C. | 可用KI一淀粉试纸和食醋鉴别NaNO2和NaCl | |
| D. | 实验室可用NaNO2和NH4Cl溶液混合加热制取氮气 |
