题目内容
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有
Ti和
Ti两种原子,其基态原子的电子排布式为 ;按电子排布Ti元素在元素周期表分区中属于 区元素.
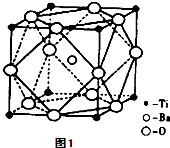
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如图1所示,它的化学式是 .
(3)氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金装饰的替代品.以TiCl4为原料,经过一系列反应,可以制得Ti3N4和纳米TiO2.
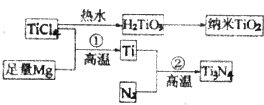
①TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为 .②纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如下:
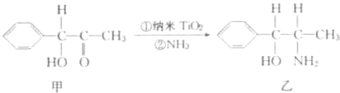
化合物甲的分子中采取sp2杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 .
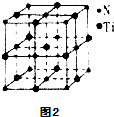
③另有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中含有 个N原子,晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为 g?cm-3(用NA表示阿伏加德罗常数的数值,只列算式).
(1)钛有
48 22 |
50 22 |
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如图1所示,它的化学式是

(3)氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金装饰的替代品.以TiCl4为原料,经过一系列反应,可以制得Ti3N4和纳米TiO2.

①TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为

化合物甲的分子中采取sp2杂化的碳原子个数为
③另有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中含有

考点:晶胞的计算,原子核外电子排布,判断简单分子或离子的构型
专题:化学键与晶体结构
分析:(1)根据核外电子排布规律和元素周期表可以解决问题;
(2)利用均摊法可知化学式;
(3)①、根据中心原子的杂化方式可知分子的空间构型,②、根据化合物甲的结构可知碳的杂化方式,根据化合物乙的结构可知sp3杂化的原子种类,再根据元素周期律比较第一电离能,③、利用均摊法算出N原子个数,根据晶胞的质量和体积求得密度.
(2)利用均摊法可知化学式;
(3)①、根据中心原子的杂化方式可知分子的空间构型,②、根据化合物甲的结构可知碳的杂化方式,根据化合物乙的结构可知sp3杂化的原子种类,再根据元素周期律比较第一电离能,③、利用均摊法算出N原子个数,根据晶胞的质量和体积求得密度.
解答:
解:(1)根据
Ti可知,钛为22号元素,所以它电子排布式为:1s22s22p63s23p63d24s2,它在元素周期表的第四周期第ⅡB族,所以是d区元素,故答案为:1s22s22p63s23p63d24s2; d;
(2)利用均摊法可知Ti的原子个数为:8×
=1,Ba的原子个数为:1,O的原子个数为:12×
=3,所以晶体的化学式为:BaTiO3,故答案为:BaTiO3;
(3))①、TiCl4分子中4个氯原子不在同一平面上,可知Ti原子的杂化方式为sp3,所以分子的空间构型为正四面体,故答案为:正四面体;
②化合物甲的分子中采取sp2杂化的碳原子有苯环上的六个各羰基中的一个,共7个,根据化合物乙的结构可知sp3杂化的原子有羟基中的氧、氨基中的氮、碳链上的三个碳,它们都位于第二周期,C、N、O 原子序数依次增加,根据元素周期律,同周期元素随着原子序数依次增加电负性逐渐增大,所以它们的电负性关系为:O>N>C,故答案为:7; O>N>C;
③根据均摊法可算出该晶胞中N原子个数为:6×
+8×
=4,该晶胞中Ti原子个数为:1+12×
=4,∴晶胞的质量m=
,而晶胞的体积V=(2a×10-10)3cm3,所以晶体的密度ρ=
=
g?cm-3,故答案为:4=
.
48 22 |
(2)利用均摊法可知Ti的原子个数为:8×
| 1 |
| 8 |
| 1 |
| 4 |
(3))①、TiCl4分子中4个氯原子不在同一平面上,可知Ti原子的杂化方式为sp3,所以分子的空间构型为正四面体,故答案为:正四面体;
②化合物甲的分子中采取sp2杂化的碳原子有苯环上的六个各羰基中的一个,共7个,根据化合物乙的结构可知sp3杂化的原子有羟基中的氧、氨基中的氮、碳链上的三个碳,它们都位于第二周期,C、N、O 原子序数依次增加,根据元素周期律,同周期元素随着原子序数依次增加电负性逐渐增大,所以它们的电负性关系为:O>N>C,故答案为:7; O>N>C;
③根据均摊法可算出该晶胞中N原子个数为:6×
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 4 |
| 4×62 |
| NA |
| m |
| V |
| 62×4 |
| (2a×10-10)3NA |
| 62×4 |
| (2a×10-10)3NA |
点评:本题主要考查了原子核外电子排布、元素周期表、轨道杂化、分子的空间构型及晶胞的计算,考查的内容难度中等.

练习册系列答案
相关题目
下列关于浓硫酸的叙述正确的是( )
| A、浓H2SO4有氧化性,稀H2SO4无氧化性 |
| B、常温下能用铝制容器盛放浓硫酸 |
| C、浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 |
| D、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
K2FeO4可用于净水.K2FeO4中Fe元素的化合价为( )
| A、+2 | B、+3 | C、+4 | D、+6 |
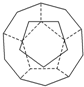 德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.
德国和美国科学家首先制出由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成如图.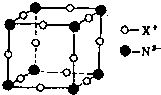 氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物.
氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物.