题目内容
7.无色溶液中能大量共存的是( )| A. | Cu2+、Cl-、SO42-、K+ | B. | K+、OH-、CO32-、Na+ | ||
| C. | HCO3-、OH-、Cl-、Na+ | D. | Ag+、NO3-、Cl-、K+ |
分析 无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.铜离子为有色离子;
B.四种离子之间不发生反应,都是无色离子;
C.碳酸氢根离子与氢氧根离子反应;
D.银离子与氯离子反应生成氯化银沉淀.
解答 解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.Cu2+为有色离子,不满足溶液无色的条件,故A错误;
B.K+、OH-、CO32-、Na+之间不反应,且都是无色离子,在溶液中能够大量共存,故B正确;
C.HCO3-、OH-之间发生反应,在溶液中不能大量共存,故C错误;
D.Ag+、Cl-之间反应生成难溶物氯化银,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
18.下列有关物质用途的叙述不正确的是( )
| A. | 单质硅是光导纤维的主要成分 | B. | 氯气可用于自来水杀菌消毒 | ||
| C. | 氧化铁常用作红色油漆和涂料 | D. | 过氧化钠可用作潜艇里氧气的来源 |
2.将a g镁铝合金投入到x mL 1mol/L的盐酸中,金属完全溶解,再加入y mL 2mol/L NaOH溶液,沉淀达到最大值,质量为(a+3.4)g,则下列说法不正确的是( )
| A. | 镁铝合金与盐酸反应转移电子数为0.2NA | |
| B. | x=2y | |
| C. | 沉淀为Mg(OH)2和Al(OH)3的混合物 | |
| D. | a的取值范围为0.9<a<1.2 |
19.下列关于浓硫酸和浓硝酸的叙述正确的是( )
| A. | 浓硫酸和浓硝酸均具有强氧化性 | |
| B. | 浓硫酸和浓硝酸长期露置在空气中浓度均会增大 | |
| C. | 常温下浓硫酸和浓硝酸均不能用铝制容器贮存 | |
| D. | 浓硫酸和浓硝酸常温下均可以与Cu迅速反应 |
16.下列叙述不正确的是( )
| A. | Na、Mg、Al元素最高化合价依次升高 | B. | P、S、Cl原子半径依次减小 | ||
| C. | N、O、F元素非金属性依次减弱 | D. | Li、Na、K原子的电子层数依次增多 |
17.已知某气态化石燃料X中只含有碳、氢两种元素,为探究该气体中碳和氢两种元素的质量比,某同学设计了燃烧法测量的实验方案,通过测量装置C和D的增重即可求得碳和氢两种元素的质量比.实验装置如下图所示(已知CuO 可以作为碳氢化合物燃烧的催化剂):
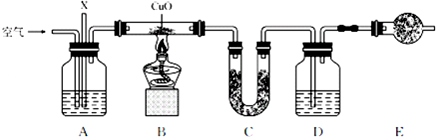
(1)若A装置中所盛放的药品是浓NaOH 溶液,装置A的作用有:
①除去空气中的CO2气体;
②调节X和空气的通入速率,保证O2过量
(2)D装置中所盛放的药品是浓NaOH溶液,
(3)E装置的作用是防止空气中的二氧化碳和水蒸气进入装置D,对结果产生影响,
(4)上述装置中有一处缺陷,请改正在A、B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管.
(5)若实验装置经过改正后,得到的实验数据如下:
则该气体中碳和氢两种元素的质量比为3:1.

(1)若A装置中所盛放的药品是浓NaOH 溶液,装置A的作用有:
①除去空气中的CO2气体;
②调节X和空气的通入速率,保证O2过量
(2)D装置中所盛放的药品是浓NaOH溶液,
(3)E装置的作用是防止空气中的二氧化碳和水蒸气进入装置D,对结果产生影响,
(4)上述装置中有一处缺陷,请改正在A、B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管.
(5)若实验装置经过改正后,得到的实验数据如下:
| 质量 | 实验前 | 实验后 |
| 药品+U形管的质量/g | 101.1 | 102.9 |
| 药品+广口瓶D的质量/g | 312.0 | 314.2 |
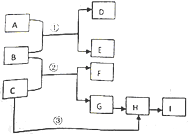 下列框图中物质均为中学化学常见物质.已知A、B、C均为有刺激性气味气体,A、B分别通入品红溶液中,红色均褪去;B、C分别通入紫色石蕊试液中,B使溶液先变红后褪色,C使溶液显蓝色;H为无色气体,I为红棕色气体,反应②有大量白烟生成.
下列框图中物质均为中学化学常见物质.已知A、B、C均为有刺激性气味气体,A、B分别通入品红溶液中,红色均褪去;B、C分别通入紫色石蕊试液中,B使溶液先变红后褪色,C使溶液显蓝色;H为无色气体,I为红棕色气体,反应②有大量白烟生成.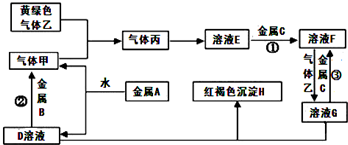 有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属.三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出).
有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属.三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出).