题目内容
在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g.此混合气体中C和O两种原子的物质的量之比为( )
| A、4:3 | B、3:4 |
| C、2:1 | D、1:2 |
考点:物质的量的相关计算
专题:
分析:根据n=
计算混合气体的物质的量,令CO和CO2的物质的量分别为xmol、ymol,节主题及关系和质量关系求得x、y,再根据二者物质的量计算出混合气体中C和O两种原子的物质的量之比.
| V |
| Vm |
解答:
解:在标准状况下,13.44LCO和CO2组成的混合气体的物质的量为
=0.6mol,
令CO和CO2的物质的量分别为xmol、ymol,则:x+y=0.6,28x+44y=20,
解得:x=0.4,y=0.2.
所以混合气体中C和O两种原子的物质的量之比为(0.4+0.2):(0.4+2×0.2)=3:4;
故选B.
| 13.44L |
| 22.4L/mol |
令CO和CO2的物质的量分别为xmol、ymol,则:x+y=0.6,28x+44y=20,
解得:x=0.4,y=0.2.
所以混合气体中C和O两种原子的物质的量之比为(0.4+0.2):(0.4+2×0.2)=3:4;
故选B.
点评:本题考查化学计算,难度不大,可以利用题干中的量的关系进行计算.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
下列溶液中Cl-浓度最大的是( )
| A、1L0.1mol/LKCl溶液 |
| B、0.2L0.2mol/L的盐酸溶液 |
| C、0.1L0.1mol/L的AlCl3溶液 |
| D、0.3L0.1 mol/L的MgCl2溶液 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、H2SO4 |
| B、C2H5OH |
| C、NH4SO4 |
| D、SO2 |
在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中氧化剂与还原剂的物质的量之比是( )
| A、1:1 | B、3:8 |
| C、2:3 | D、8:3 |
下列说法中正确的是(NA表示阿伏加德罗常数的值)( )
| A、常温下,28gFe与足量的浓硝酸反应,转移的电子数为1.5NA |
| B、标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2 |
| C、3.2g铜在硫蒸气中完全燃烧,转移的电子数为0.1NA |
| D、常温常压下,0.1mol氖气含有的电子数为NA |
下列反应中生成物总能量高于反应物总能量的是( )
| A、乙醇燃烧 |
| B、氯酸钾分解制氧气 |
| C、铝片和盐酸反应 |
| D、氧化钙溶于水 |
下列说法不正确的是( )
| A、分散质粒子直径介于1~100 nm之间的分散系称为胶体 |
| B、江河入海口三角洲的形成通常与胶体的性质有关 |
| C、用激光笔检验淀粉溶液的丁达尔效应 |
| D、向煮沸的1 mol?L-1 NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 |
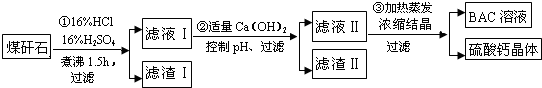
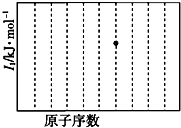 a~e是元素周期表中前四周期元素,请根据表中信息回答下列问题:
a~e是元素周期表中前四周期元素,请根据表中信息回答下列问题: