题目内容
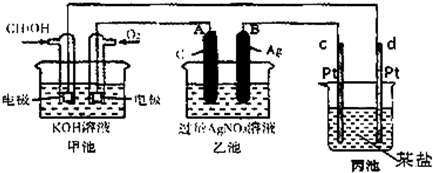
16.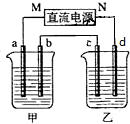 如图所示装置中,甲、乙两个烧杯分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙两个烧杯分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得甲中NaOH浓度为6.25%,乙中c电极质量增加.
据此回答问题:
(1)电源的N端为正极;
(2)电极b上发生的电极反应为4OH--4e-=2H2O+O2↑;
(3)电极c的质量变化是71.1g.
分析 (1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明c电极是电解池阴极,则d电极是阳极,连接电解池阳极的原电池电极N是正极;
(2)电解氢氧化钠溶液时,b为阳极,阳极上氢氧根离子放电生成氧气;
(3)根据NaOH的浓度变化求出电解的水的物质的量,根据电子守恒计算c的质量变化.
解答 解:(1)该装置是电解池,接通电源,经过一段时间后,乙中c电极质量增加,说明C电极是电解池阴极,则d电极是阳极,连接电解池阳极的原电池电极是正极,所以N是原电池正极,故答案为:正;
(2)电解氢氧化钠溶液时,b为阳极,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
(3)设电解的水的质量为xg,则100g×5.00%=(100-x)g×6.25%,解得x=20,甲中反应2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,乙中反应2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+,由电子守恒可知:2H2O~4e-~2Cu
2×18 2×64
20g m
则m=$\frac{20g×2×64}{2×18}$=71.1g;
故答案为:71.1.
点评 本题考查了原电池原理的应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意两个电解池为串联电路,各电极上得失电子的数目相等.做题时要正确写出电极方程式,准确判断两极上离子的放电顺序,题目难度中等.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
6.在一恒压密闭容器中充入1mol NO2建立如下平衡:2NO2?N2O4,此时NO2的转化率为x%,在其他条件不变的条件下,再充入1mol NO2,待新平衡建立时测得NO2的转化率为y%,则大小关系正确的是( )
| A. | x<y | B. | x=y | C. | x>y | D. | 无法确定 |
11.关于如图所示装置的叙述,正确的是( )
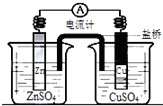

| A. | 铜是阳极,铜片上有气泡产生 | |
| B. | 锌离子在锌片表面被还原 | |
| C. | 正极附近的SO${\;}_{4}^{2-}$离子浓度逐渐增大 | |
| D. | 盐桥中的阳离子会移向CuSO4溶液 |
8.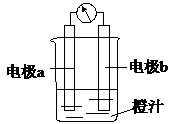 课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成.下列结论不正确的是( )
课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成.下列结论不正确的是( )
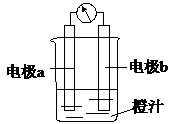 课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成.下列结论不正确的是( )
课堂学习中,同学们利用镁条、锌片、铜片、导线、电流计、橙汁、烧杯等用品探究原电池的组成.下列结论不正确的是( )| A. | 原电池是将化学能转化成电能的装置 | |
| B. | 原电池由电极、电解质溶液和导线等组成 | |
| C. | 右图中a极为镁条、b极为锌片时,导线中会产生电流 | |
| D. | 右图中a极为锌片、b极为铜片时,电子由铜片通过导线流向锌片 |
5.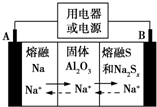 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )
 钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示.下列说法正确的是( )| A. | 放电时,电极A为负极,Na+由B向A移动 | |
| B. | 放电时,负极反应式为2Na-xe-═2Na+ | |
| C. | 充电时,电极B的反应式为S2--2e-═xS | |
| D. | 充电时,电极B接电源的负极 |
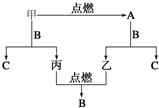 甲、乙、丙三种常见单质,A、B、C是三种常见的化合物,A为淡黄色固体,它们之间的转化关系如图所示.
甲、乙、丙三种常见单质,A、B、C是三种常见的化合物,A为淡黄色固体,它们之间的转化关系如图所示.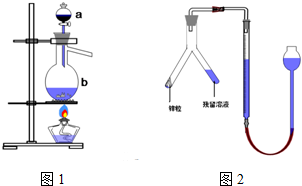
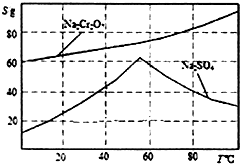 实验室模拟用铬铁矿(主要成分是FeO•Cr2O3)制备红矾钠(Na2Cr2O7•2H20).
实验室模拟用铬铁矿(主要成分是FeO•Cr2O3)制备红矾钠(Na2Cr2O7•2H20).