题目内容
欲配置物质的量浓度为0.60mol/L的MgCl2溶液500mL,回答下列问题:
(1)根据计算,所需的质量为 g,如果某同学称量时将砝码放在左盘,而将药品放在右盘(天平最小砝码为5g),则实际称取质量为 g;
(2)要配制上述溶液,所需仪器除天平、药匙、烧杯、玻璃棒外,还要 .
(1)根据计算,所需的质量为
(2)要配制上述溶液,所需仪器除天平、药匙、烧杯、玻璃棒外,还要
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)依据m=CVM计算需要溶质的质量,根据天平的使用规则:左盘的质量=右盘的质量+游码的质量解答;
(2)依据配制一定物质的量浓度溶液的一步步骤选择所需的仪器.
(2)依据配制一定物质的量浓度溶液的一步步骤选择所需的仪器.
解答:
解:(1)配制物质的量浓度为0.60mol/L的MgCl2溶液500mL,需要氯化镁的质量m=0.6mol/L×0.5L×95g/mol=28.5g;当天平最小砝码为5克,3.5
g用游码表示,要称量28.5g氯化镁,应使用25g砝码,3.5g游码,根据天平的使用规则:左盘的质量=右盘的质量+游码的质量可知:砝码与游码颠倒后,砝码的质量=物的质量+游码的质量,则物的质量=砝码质量-游码质量=25g-3.5g=21.5g,
故答案为:28.5;21.5;
(2)配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量固体,把氯化镁倒入烧杯进行溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、天平、药匙、烧杯、胶头滴管、500mL容量瓶,所以还需要胶头滴管、500mL容量瓶;
故答案为:胶头滴管、500mL容量瓶.
g用游码表示,要称量28.5g氯化镁,应使用25g砝码,3.5g游码,根据天平的使用规则:左盘的质量=右盘的质量+游码的质量可知:砝码与游码颠倒后,砝码的质量=物的质量+游码的质量,则物的质量=砝码质量-游码质量=25g-3.5g=21.5g,
故答案为:28.5;21.5;
(2)配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量固体,把氯化镁倒入烧杯进行溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、天平、药匙、烧杯、胶头滴管、500mL容量瓶,所以还需要胶头滴管、500mL容量瓶;
故答案为:胶头滴管、500mL容量瓶.
点评:本题考查了一定物质的量浓度溶液的配制,明确配制的原理和步骤是解题关键,注意托盘天平称量固体的原理,题目难度不大.

练习册系列答案
相关题目
下列电离方程式中,正确的是( )
| A、NaOH═Na++OH- |
| B、2H2O═O2↑+2H2↑ |
| C、H2SO4═H2++SO42- |
| D、Na2CO3═2Na++OH- |
某气态烃0.5mol恰好与1molHCl加成,生成物分子中的氢又可被3molCl2取代,则此气态烃可能是( )
| A、C2H2 |
| B、C2H4 |
| C、CH2=C(CH3)2 |
| D、CH≡C-CH3 |
下列有关溶液组成的描述合理的是( )
| A、常温下,水电离出的c(H+)=1×10-12mol/L,某无色溶液中不可能大量存在:Al3+、NH4+、Cl-、S2- |
| B、pH=2的溶液中,可能大量存在:Na+、Fe2+、ClO-、SO42- |
| C、常温下某溶液中KW/c(H+)=1×10-12,溶液中可能大量存在:Na+、NH4+、Cl-、HCO3- |
| D、某溶液中加入少量Al 有气体生成,溶液中可能大量存在:Na+、K+、Cl-、NO3- |
一定条件下的密闭容器中有如下反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.9kJ?mol-1,下列叙述正确的是( )
| A、当NH3、O2、NO、H2O浓度比为4:5:4:6时达到平衡 | ||
B、平衡时v正(O2)=
| ||
| C、平衡后减小压强,混合气体平均摩尔质量增大 | ||
| D、平衡后升高温度,混合气体中NO含量降低 |
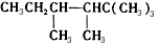
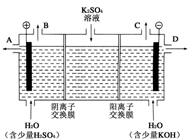 电化学知识是化学反应原理的重要部分,以下是常见的电化学装置:
电化学知识是化学反应原理的重要部分,以下是常见的电化学装置: