题目内容
可待因(codeine)可用于治疗咳嗽,是一种一元弱碱,Kb=2×10-6则0.020mol?L-1的可待因溶液中的c(OH-)约为(已知
≈1.414)( )
| 2 |
| A、2×10-4mol?L-1 |
| B、2×10-8mol?L-1 |
| C、1.414×10-3mol?L-1 |
| D、1×10-3mol?L-1 |
考点:弱电解质在水溶液中的电离平衡
专题:计算题
分析:设化学式为MOH,发生MOH?M++OH-,已知电离平衡常数以及碱的浓度,结合Kb=
计算.
| c(M+)×c(OH-) |
| c(MOH) |
解答:
解:设化学式为MOH,发生MOH?M++OH-,
则Kb=
=2×10-6,
c(OH-)=c(M+)=
≈
mol/L=2×10-4mol?L-1,
故选A.
则Kb=
| c(M+)×c(OH-) |
| c(MOH) |
c(OH-)=c(M+)=
| 2×10-6×c(MOH) |
| 2×10-6×0.020 |
故选A.
点评:本题考查弱电解质的电离,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握计算公式的运用,难度不大.

练习册系列答案
相关题目
已知反应:2SO2(g)+O2(g)
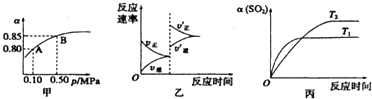
2SO3(g)△H<0某温度下,将2molSO2 和1molO2置于密闭容器中,反应到达平衡后,SO2的平衡转化率(a)与体系总压强(ρ)的关系如图甲所示,则下列说法正确的是( )
| 催化剂 |
| △ |

| A、由图甲知,A点SO2的平衡浓度为0.4 mol/L |
| B、点SO2、O2、SO3的平衡浓度之比为2:1:2 |
| C、达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D、压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
Mg、Cu和Al三种金属粉末的混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量NaOH溶液,再过滤,滤液中存在的离子有( )
| A、AlO2- |
| B、Al3+ |
| C、Mg2+ |
| D、Cu2+ |
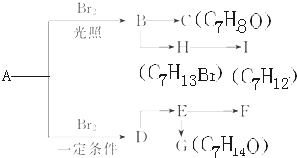
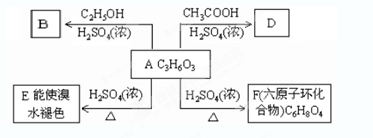
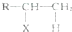 .A、B、C、D、E、M、N有下列转化关系:
.A、B、C、D、E、M、N有下列转化关系: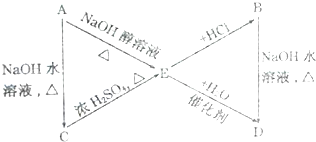
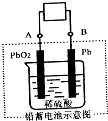 CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是