题目内容
6.下列说法正确的是( )| A. | 乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 | |
| B. | 烃与卤素单质之间的反应均为加成反应 | |
| C. | 多糖、油脂均可发生水解反应 | |
| D. | 石油分馏和裂化均为物理变化 |
分析 A.聚乙烯中不含碳碳双键;
B.烷烃与卤素单质发生取代反应;
C.多糖水解生成葡萄糖,油脂水解生成高级脂肪酸(或盐)与甘油;
D.裂化为大分子生成小分子的反应.
解答 解:A.聚乙烯中不含碳碳双键,与高锰酸钾不反应,而乙烯可使酸性高锰酸钾溶液褪色,故A错误;
B.烷烃与卤素单质发生取代反应,不饱和烃与卤素单质发生加成反应,故B错误;
C.多糖水解生成葡萄糖,油脂水解生成高级脂肪酸(或盐)与甘油,则二者均发生水解反应,故C正确;
D.裂化为大分子生成小分子的反应,为化学变化,石油分馏为物理变化,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、油脂等有机物性质的考查,注意选项D为解答的易错点,题目难度不大.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
16.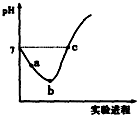 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )| A. | 实验进程中可用pH试纸测定溶液的pH | |
| B. | a点的溶液中:c(H+)=c(Cl-)+c(HClO)+c(OH-) | |
| C. | 由a点到b点的过程中,溶液中C(H+):C(ClO-)减小 | |
| D. | c点所示溶液中:c(Na+)=2c(ClO-)+c(HClO) |
17.化学是材料科学发展的基础.下列说法正确的是( )
| A. | 可用作荧光灯内壁保护层的氧化铝纳米材料属于胶体 | |
| B. | 高分子材料可能导电,如聚乙炔 | |
| C. | 钢化玻璃、有机玻璃、防弹玻璃均属于硅酸盐材料 | |
| D. | 人造刚玉的主要成分是MgO,熔点很高,可用作高级耐火材料 |
14.某学习小组在实验室研究SO2与Ba(NO3)2溶液的反应:
实验:向盛有2mL 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色.
探究1:白色沉淀产生的原因.
(1)白色沉淀是BaSO4.
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2.
①支持甲同学观点的实验证据是液面上方略显浅棕色.
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO+4H+.
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
探究2:在氧化SO2的过程中,NO3-和O2哪种微粒起到了主要作用.
(3)图1,在无氧条件下,BaCl2溶液pH下降的原因是SO2+H2O?H2SO3,H2SO3?HSO3-+H+.
(4)图2,BaCl2溶液中发生反应的离子方程式为2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+.
(5)依据上述图象你得出的结论是在氧化SO2的过程中,O2起了主要作用.
实验:向盛有2mL 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生,液面上方略显浅棕色.
探究1:白色沉淀产生的原因.
(1)白色沉淀是BaSO4.
(2)分析白色沉淀产生的原因,甲同学认为是NO3-氧化了SO2,乙同学认为是溶液中溶解的O2氧化了SO2.
①支持甲同学观点的实验证据是液面上方略显浅棕色.
②依据甲的推断,请写出Ba(NO3)2溶液与SO2反应的离子方程式3Ba2++2NO3-+3SO2+2H2O=3BaSO4↓+2NO+4H+.
③乙同学通过下列实验证明了自己的推测正确,请完成实验方案:
| 实验操作 | 实验现象 |
| 向2mL 0.1mol/LBaCl2 溶液(填化学式)中通入SO2 | 试管内有白色沉淀产生 |
| 实验操作 | 实验数据 |
| 向烧杯中加入煮沸了的0.1mol/L的BaCl2溶液25mL,再加入25mL植物油,冷却至室温,用pH传感器测定溶液pH随时间(t)的变化曲线 | 图1:向BaCl2(无氧)溶液中通入SO2 |
| 向烧杯中分别加入25mL 0.1mol/L的BaCl2溶液、Ba(NO3)2溶液,通入SO2,用pH传感器分别测定溶液pH随时间(t)变化的曲线. | 图2:分别向BaCl2、Ba(NO3)2溶液中通入SO2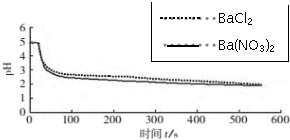 |
(4)图2,BaCl2溶液中发生反应的离子方程式为2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+.
(5)依据上述图象你得出的结论是在氧化SO2的过程中,O2起了主要作用.
1.锌溴液流电池用溴化锌溶液作电解液,并在电池间不断循环.下列有关说法正确的是( )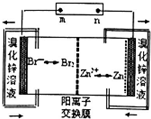

| A. | 充电时Zn2+通过阳离子交换膜由左侧流向右侧 | |
| B. | 放电时每转移2mol电子负极增重130g | |
| C. | 充电时阴极的电极反应式为Br2+2e-=2Br- | |
| D. | 若将电解液改为氯化锌溶液放电效果更好更安全 |
11.化学与生活、社会发展息息相关,下列说法不正确的是( )
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| D. | 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金 |
16.下列物质放置在空气中均会变质,下列关于检验是否变质的操作方法与结论均正确的是( )
| 选项 | 物质 | 操作 | 现象 | 结论 |
| A | 甲醛溶液 | 加紫色石蕊溶液 | 变红 | 变质 |
| B | 亚硫酸钠溶液 | 加BaCl2 | 产生白色沉淀 | 变质 |
| C | 铁粉 | 加KSCN | 未变血红色 | 未变质 |
| D | 过氧化钠固体 | 加足量水 | 产生使带火星木条复燃的气体 | 未变质 |
| A. | A | B. | B | C. | C | D. | D |





 ;
; ;
; ;
; .
.