题目内容
(共8分)
Ⅰ.(2分)已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得溶液呈酸性;0.01 mol?L-1的HIO3或HMnO4溶液与pH=12的Ba(OH)2溶液等体积混合所得溶液均呈中性。
(1)H5IO6是 (填“强电解质”或“弱电解质”)。
(2)(6分)已知H5IO6和MnSO4在溶液中反应生成高锰酸、碘酸和硫酸,此反应中氧化剂是 (填化学式)。
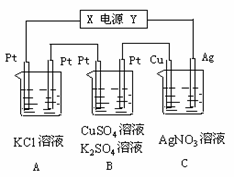
Ⅱ.如图所示,若电解5min时铜电极质量增加2.16g,B池的两极都有气体产生。
 试回答:
试回答:
⑴ 电源电极X名称为____________。
⑵ pH变化:A池________________,
B池________________,
C池________________。
⑶ 写出B池中所发生的电解反应方程式:
_____________________________________________________________________。
Ⅰ.(1)弱电解质 (2)H5IO6
Ⅱ.(1)负极(2)增大;减小;不变
2CuSO4+2H2O=====2Cu+O2↑+2H2SO4
2H2O=====2H2↑+O2↑

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案(共8分,每空1分)看下列仪器装置图,回答下列问题: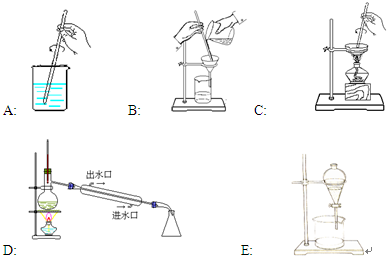
(1)写出上述各装置的名称:
| A.; | B.; | C.; |
| D.;E. |
①酒精和水: ②食盐和水:
③花生油和水:
(共8分)
在2 L恒容密闭容器中,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)如图中表示NO2的变化的曲线是 。
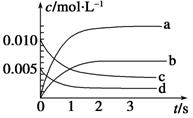
(2)求 2 s末用氧气表示的平均反应速率v(O2)=
(3)求达平衡时NO的转化率为
(4)能说明该反应已经达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v(NO)逆=2v(O2)正 d.容器内的密度保持不变
(5)能够使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离出NO2气体 b.增大O2的浓度