题目内容
11.常温下,下列有关叙述正确的是( )| A. | 在0.1mol/L Na2C2O4中:2c(Na+)═c(C2O42- )+c(HC2O4-)+c(H2C2O4) | |
| B. | 浓度均为0.1mol/L的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c〔HCO3-) | |
| C. | 向10mL pH=l2的NaOH溶液中滴加等体积pH=2的CH3COOH:c(CH3COO-)>c(Na+)>c(OH-)>C(H+) | |
| D. | 0.2mol/L NaHCO3与0.1mol/L KOH溶液等体积混合:c(Na+)═2c(CO32-)+c〔HCO3-)+c(H2CO3) |
分析 A.根据草酸钠溶液中的物料守恒判断;
B.二者恰好反应生成碳酸钠溶液,根据碳酸钠溶液中的电荷守恒判断;
C.醋酸为弱酸,混合液中醋酸过量,溶液呈酸性,则c(H+)>c(OH-);
D.钠元素和C元素的总物质的量不变,根据物料守恒判断.
解答 解:A.在0.1mol/L Na2C2O4中,根据物料守恒可得:c(Na+)═2c(C2O42- )+2c(HC2O4-)+2c(H2C2O4),故A错误;
B.浓度均为0.1mol/L的小苏打溶液与烧碱溶液等体积混合,反应生成碳酸钠溶液,根据电荷守恒可得:c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c〔HCO3-),故B正确;
C.向10mL pH=l2的NaOH溶液中滴加等体积pH=2的CH3COOH,醋酸过量,溶液呈酸性,则(H+)>c(OH-),根据电荷守恒可知:c(CH3COO-)>c(Na+),溶液中离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D.0.2mol/L NaHCO3与0.1mol/L KOH溶液等体积混合,根据物料守恒可得:c(Na+)═c(CO32-)+c〔HCO3-)+c(H2CO3),故D错误;
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理的含义及应用方法,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
相关题目
1.脲醛塑料(UF),俗称“电玉”,可制得多种制品,如日用品、电器元件等,在一定条件下合成脲醛塑料的反应如下,下列说法中正确的是( )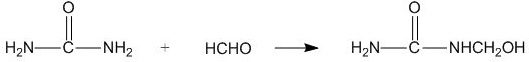
(尿素)
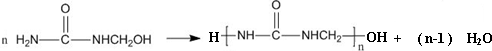
(电玉)

(尿素)

(电玉)
| A. | 合成脲醛塑料的反应为加聚反应 | |
| B. | 尿素与氰酸铵 ( NH4CNO ) 互为同系物 | |
| C. | 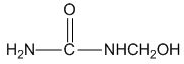 能发生水解反应 能发生水解反应 | |
| D. | 脲醛塑料平均相对分子质量为10000,平均聚合度为111 |
6.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素.下列说法正确的是( )
| A. | B的单质在自然界只有一种核素 | |
| B. | 元素C、D、E的简单离子的半径依次减小 | |
| C. | E的单质氧化性最强 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
16.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 是酚酞变红色的溶液:K+、Fe3+、SO42-、Cl- | |
| B. | 水电离的c(H+)=1×10-13mol/L的溶液中:K+、Na+、AlO2-、CO32- | |
| C. | 与Al反应能放出H2的溶液中:Fe2+、Na+、NO3-、SO42- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=1×10-13mol/L的溶液中:NH4+、Cu2+、Cl-、NO3- |
3.铁元素是重要的金属元素,铁单质及化合物在工业和生活中也有广泛的用途.
(1)在实验室中,FeCl2可用铁粉和盐酸反应制备,FeCl3可用铁粉和氯气反应制备.
(2)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3与KClO在强碱性条件下反应制取K2FeO4,其反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.与MnO2-Zn电池类似,K2FeO4-Zn也可组成碱性电池,该电池的总反应的离子方程式为3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.
(3)铁与水反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H<0上述反应的平衡常数表达式K=$\frac{[{H}_{2}]{\;}^{4}}{[{H}_{2}O]^{4}}$.
(4)若在2L恒容绝热(不与外界交换能量)装置中,按下表充入起始物质,起始时与平衡后的物质的物质的量见下表:
达平衡后,若再加入四种物质,各物质的物质的量如下表:
当重新达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是B>C>A(用A、B、C表示).
(5)已知常温下:Fe(OH)3的Ksp[Fe(OH)3]=1.0×10-39,Ksp[Mg(OH)2]=1.0×10-12,若将MgCl2、FeCl3均为0.1mol•L-1混合溶液中的pH用MgO调节至pH=4,则溶液中$\frac{c(M{g}^{2+})}{c(F{e}^{3+})}$比值约为108.
(1)在实验室中,FeCl2可用铁粉和盐酸反应制备,FeCl3可用铁粉和氯气反应制备.
(2)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3与KClO在强碱性条件下反应制取K2FeO4,其反应的离子方程式为2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.与MnO2-Zn电池类似,K2FeO4-Zn也可组成碱性电池,该电池的总反应的离子方程式为3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.
(3)铁与水反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H<0上述反应的平衡常数表达式K=$\frac{[{H}_{2}]{\;}^{4}}{[{H}_{2}O]^{4}}$.
(4)若在2L恒容绝热(不与外界交换能量)装置中,按下表充入起始物质,起始时与平衡后的物质的物质的量见下表:
| Fe | H2O(g) | Fe3O4 | H2 | |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| Fe | H2O(g) | Fe3O4 | H2 | |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1.0 | 4.0 |
| C/mol | m | n | p | q |
(5)已知常温下:Fe(OH)3的Ksp[Fe(OH)3]=1.0×10-39,Ksp[Mg(OH)2]=1.0×10-12,若将MgCl2、FeCl3均为0.1mol•L-1混合溶液中的pH用MgO调节至pH=4,则溶液中$\frac{c(M{g}^{2+})}{c(F{e}^{3+})}$比值约为108.
6.t℃时,AgCl 的 Ksp=2×10-10;Ag2CrO4是一种橙红色固体,在水中的沉淀溶解平衡曲 线如图所示.下列说法正确的是( )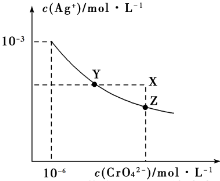

| A. | 在 t℃时,AgCl 的溶解度大于 Ag2CrO4 | |
| B. | 在 t℃时,Ag2CrO4的 Ksp=1×10-1210-3 | |
| C. | 在饱和 Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点到X 点 | |
| D. | 在 t℃时,用 AgNO3 标准溶液滴定 20mL 未知浓度的 KCl 溶液,不能采用K2CrO4溶液为指示剂 |
7.用等体积的0.1mol•L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液中的SO42-完全沉淀,则三种硫酸盐的物质的量浓度之比为( )
| A. | 3:2:3 | B. | 3:1:2 | C. | 2:6:3 | D. | 1:1:1 |

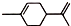 ),则A的系统命名是2-甲基-1,3-丁二烯.在合成M的过程中还可以生成M的一种同分异构体,其结构简式为
),则A的系统命名是2-甲基-1,3-丁二烯.在合成M的过程中还可以生成M的一种同分异构体,其结构简式为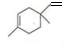 .
.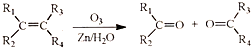 (R1、R2、R3、R4为烃基或氢原子)
(R1、R2、R3、R4为烃基或氢原子)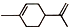 )发生上述反应的产物中分子量较大的结构简式
)发生上述反应的产物中分子量较大的结构简式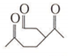 .
.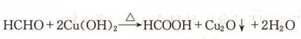 .
.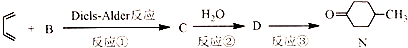
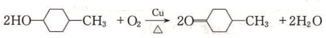 .
.