题目内容
4.核外电子排布相同的一组微粒是( )| A. | Mg2+、Al3+、F-、Ne | B. | Na+、F-、S2-、Ar | ||
| C. | K+、Ca2+、S2-、Ne | D. | Mg2+、Na+、Cl-、S2- |
分析 A.四种粒子的核外电子总数都是10,核外电子排布相同;
B.Na+、F-的核外电子总数为10,S2-、Ar的核外电子总数为18;
C.K+、Ca2+、S2-,的核外电子总数为18,Ne核外电子总数为10;
D.Mg2+、Na+核外电子总数为10,Cl-、S2-的核外电子总数为18.
解答 解:A.Mg2+、Al3+、F-、Ne的核外电子总数都是10,核外电子排布都是2、8,相满足条件,故A正确;
B.Na+、F-的核外电子总数为10,核外电子排布,是2、8,S2-、Ar的核外电子总数为18,核外电子排布不完全相同,故B错误;
C.K+、Ca2+、S2-,的核外电子总数为18,核外电子排布是2、8、8,Ne核外电子总数为10,核外电子排布,是2、8,故C错误;
D.Mg2+、Na+核外电子总数为10,核外电子排布,是2、8;Cl-、S2-的核外电子总数为18,核外电子排布是2、8、8,故D错误;
故选A.
点评 本题考查了粒子的结构及核外电子排布,题目难度中等,明确常见粒子结构与核外电子排布规律为解答关键,试题侧重基础知识的考查,试题培养了学生的灵活应用能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
14.在汽车排气管加装催化装置,可有效减少CO和NOx的排放,催化装置内发生反应为:NOx+CO$\stackrel{催化剂}{→}$N2+CO2(未配平),下列关于此反应的说法中错误的是( )
| A. | 当x=2时,每生成lmolN2,转移电子数为4mol | |
| B. | 该反应中化合价变化的有N和C元素 | |
| C. | 等物质的量N2和C02中,共用电子对的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |
15.以下反应属于氧化还原反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | 2NH4HCO3$\stackrel{△}{→}$2NH3↑+H2O+CO2↑ | ||
| C. | 4HCl+O2$\stackrel{△}{→}$2H2O+2Cl2 | D. | NaHCO3+NaHSO4═Na2SO4+CO2↑+H2O |
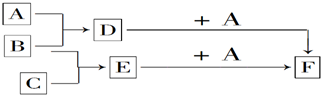
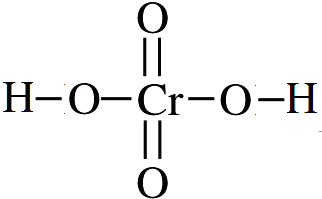 .
.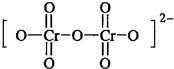
 .反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O已知反应II的产物X的溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为2S2-+5H2O=S2O32-+4H2↑+2OH-.
.反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O已知反应II的产物X的溶液中硫元素的主要存在形式为S2O32-,则II中主要反应的离子方程式为2S2-+5H2O=S2O32-+4H2↑+2OH-. 如图所示的装置,C、D、E、F都是惰性 电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答以下问题:
如图所示的装置,C、D、E、F都是惰性 电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答以下问题: