题目内容
下列反应的离子方程式正确的是( )
| A、过量氯气通入溴化亚铁溶液中:2Cl2+2Fe2++2Br-═4Cl-+2Fe3++Br2 |
B、向苯酚溶液中滴加Na2CO3溶液: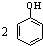 +CO32-→ +CO32-→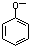 +CO2↑+H2O +CO2↑+H2O |
| C、足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- |
| D、用过量的冷氨水吸收SO2:SO2+2NH3?H2O═SO32-+2NH4++H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成氯化铁和溴;
B.二者反应生成碳酸氢钠和苯酚钠;
C.二者反应生成碳酸氢钠且有晶体析出;
D.二者反应生成亚硫酸铵.
B.二者反应生成碳酸氢钠和苯酚钠;
C.二者反应生成碳酸氢钠且有晶体析出;
D.二者反应生成亚硫酸铵.
解答:
解:A.二者反应生成氯化铁和溴,离子方程式为3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2,故A错误;
B.苯酚的酸性大于碳酸氢根离子,所以二者反应生成碳酸氢钠和苯酚钠,离子方程式为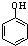 +CO32-→
+CO32-→ +HCO3-,故B错误;
+HCO3-,故B错误;
C.碳酸氢钠的溶解度小于碳酸钠,所以二者反应生成碳酸氢钠且有晶体析出,离子方程式为2Na++CO2+CO32-+H2O═2NaHCO3↓,故C错误;
D.二者反应生成亚硫酸铵,离子方程式为SO2+2NH3?H2O═SO32-+2NH4++H2O,故D正确;
故选D.
B.苯酚的酸性大于碳酸氢根离子,所以二者反应生成碳酸氢钠和苯酚钠,离子方程式为
 +CO32-→
+CO32-→ +HCO3-,故B错误;
+HCO3-,故B错误;C.碳酸氢钠的溶解度小于碳酸钠,所以二者反应生成碳酸氢钠且有晶体析出,离子方程式为2Na++CO2+CO32-+H2O═2NaHCO3↓,故C错误;
D.二者反应生成亚硫酸铵,离子方程式为SO2+2NH3?H2O═SO32-+2NH4++H2O,故D正确;
故选D.
点评:本题考查了离子方程式的书写,明确反应实质是解本题关键,并结合离子方程式书写规则解答,易错选项是C,该反应中有晶体析出,要考虑溶解度,A中要明确离子反应先后顺序,为易错点.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:4CuI+Hg═Cu2HgI4+2Cu.下列说法中正确的是( )
| A、该反应的氧化剂为CuI,氧化产物为Cu |
| B、产物Cu2HgI4中,Cu元素的化合价为+2 |
| C、当有2mol CuI参与反应时,转移电子为1mol |
| D、由Cu2+与I直接反应制得CuI的离子方程式为Cu2++I-=CuI |
已知X、Y是元素周期表中前20号元素,二者原子序数相差3,X、Y能形成化台物M,下列说法正确的是( )
| A、若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B、若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C、若M属于离子化合物,则该化合物中只存在离子键 |
| D、若M属于共价化台物,则该分子中原子个数比可能为1:2 |
X、Y、Z、W、R 5种短周期元素,其原子序数依次增大.X是元素周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A、Z与Y两种元素组成的化合物中,阴、阳离子个数比为1:1或1:2 |
| B、Y、Z、W元素形成的简单离子具有相同电子层结构,其离子半径依次增大 |
| C、Z、R元素的氧化物的水化物之间相互反应生成的盐溶液呈中性、碱性或酸性 |
| D、Y、R元素分别与X元素形成的化合物的沸点:XmY<XmR |
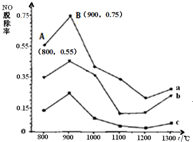 一定条件下,尿素[CO(NH2)2]与NO反应生成N2和另外2种对环境无污染的氧化物.如图是CO(NH2)2与某种烟气中NO的物质的量之比分别为1:2、2:1、3:1时,NO脱除率随温度(t)变化的图象.下列说法错误的是( )
一定条件下,尿素[CO(NH2)2]与NO反应生成N2和另外2种对环境无污染的氧化物.如图是CO(NH2)2与某种烟气中NO的物质的量之比分别为1:2、2:1、3:1时,NO脱除率随温度(t)变化的图象.下列说法错误的是( )| A、尿素脱除NO的反应为:2CO(NH2)2+6NO═2CO2+4H2O+5N2 |
| B、图中a,对应CO(NH2)2与NO的物质的量之比为1:2 |
| C、在900℃左右,NO的脱除率最佳 |
| D、NO的起始浓度为6×10-4mg/m3,图中a从A点到B点经过0.8s,这段时间内NO的脱除平均速率为1.5×10-4mg/(m3?s) |
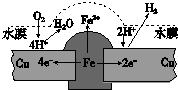 铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图.下列说法不正确的是( )
铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图.下列说法不正确的是( )| A、因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀 |
| B、若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小 |
| C、铜极上的反应是2H++2e-═H2↑,O2+4e-+4H+═2H2O |
| D、在金属表面涂一层油脂,能防止铁铆钉被腐蚀 |
下列说法不正确的是( )
| A、服用铬含量超标的药用胶囊会对人对健康造成危害 |
| B、食用一定量的油脂能促进人体对某些维生素的吸收 |
| C、CH4和Cl2在光照条件下反应的产物最多可能有四种 |
| D、无论乙烯的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关 |
下列叙述中正确的是( )
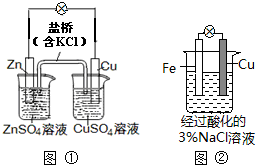

| A、图①中正极附近溶液pH降低 |
| B、图①中电子由Zn流向Cu,盐桥中的Cl-移向CuSO4溶液 |
| C、图②正极反应是O2+2H2O+4e-═4OH- |
| D、图②中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |

