��Ŀ����
4����֪��������A��B��X��Y��һ�������µ�ת����ϵ��ͼ��ʾ��
��1����AΪ�������ڽ���Ԫ�صĵ��ʣ�����NaOH��Һ��Ӧ��X�Ǻ���ɫ��ĩ����д��A��X��Ӧ�Ļ�ѧ����ʽ2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe��
��2����X�ڳ�����Ϊ��ɫҺ�壬Y�Ǿ��д��Եĺ�ɫ���壬B����̬�ǽ������ʣ���д���÷�Ӧ�Ļ�ѧ����ʽ3Fe+4H2O��g��$\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2��
���� ����ͼʾ��֪��������X�뵥��A��Ӧ���ɻ�����Y�뵥��B���÷�ӦΪ�û���Ӧ��
��1����AΪ�������ڽ���Ԫ�صĵ��ʣ�����NaOH��Һ��Ӧ����Aֻ��Ϊ����Al��X�Ǻ���ɫ��ĩ���ܹ���Al�����û���Ӧ���ɻ�����Y�͵���B����XΪFe2O3��YΪAl2O3������BΪFe���ݴ�д����Ӧ�Ļ�ѧ����ʽ��
��2����X�ڳ�����Ϊ��ɫҺ�壬��Ϊ�������XΪH2O��Y�Ǿ��д��Եĺ�ɫ���壬��YΪFe3O4��B����̬�ǽ������ʣ���XΪFe������BΪ�������ݴ�д���÷�Ӧ�Ļ�ѧ����ʽ��
��� �⣺����ͼʾ��֪��������X�뵥��A��Ӧ���ɻ�����Y�뵥��B���÷�ӦΪ�û���Ӧ��
��1����AΪ�������ڽ���Ԫ�صĵ��ʣ�����NaOH��Һ��Ӧ����AΪ����Al��X�Ǻ���ɫ��ĩ���ܹ���Al�����û���Ӧ���ɻ�����Y�͵���B����XΪFe2O3��YΪAl2O3������BΪFe����Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe��
�ʴ�Ϊ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe��
��2����X�ڳ�����Ϊ��ɫҺ�壬��Ϊ�������XΪH2O��Y�Ǿ��д��Եĺ�ɫ���壬��YΪFe3O4��B����̬�ǽ������ʣ���XΪFe������BΪ�������÷�Ӧ�Ļ�ѧ����ʽΪ��3Fe+4H2O��g�� $\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2��
�ʴ�Ϊ��3Fe+4H2O��g�� $\frac{\underline{\;\;��\;\;}}{\;}$Fe3O4+4H2��
���� ���⿼�������ƶϣ���Ŀ�Ѷ��еȣ�����ͼʾ��ȷ��Ӧ����Ϊ���ؼ���ע���������ճ���Ԫ�ؼ��仯�������ʣ���������������ѧ���ķ���������������������������

| A�� | �÷�Ӧ���ʱ�Ϊ��ֵ | |
| B�� | ��ѧ����ʽΪ NO2��g��+CO��g��?CO2��g��+NO��g�� | |
| C�� | ���£�����Ӧ���ʼ�С | |
| D�� | ����ʱ������ѹǿ��ɫ���ƽ�������ƶ� |
| A�� | ��Ȼ������Ҫ�ɷּ���ȼ��ʱ�ų�����������������Ҫ�Ķ�����Դ | |
| B�� | ����������ĸ�̼�ⵥ����������ȫ��ͬ�����ӽṹΪƽ�������� | |
| C�� | �����������Ӧ���ɵĶ��ȼ���û��ͬ���칹���� | |
| D�� | ����Ļ�ѧ���ʱȽ��ȶ��������κ����������� |
| A�� | SO2 | B�� | N2 | C�� | NH3 | D�� | NO2 |
| A�� | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2�� | |
| B�� | NH4Cl $\frac{\underline{\;\;��\;\;}}{\;}$NH3��+HCl�� | |
| C�� | 2Fe+3Cl2$\frac{\underline{\;��ȼ\;}}{\;}$2FeCl3 | |
| D�� | Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O |
| A�� | ����ˮ��ε���Al2��SO4��3��Һ�У�ֱ������ | |
| B�� | ��AlCl3��Һ����ε���NaOH��Һ��ֱ������ | |
| C�� | ��NaOH ��Һ����ε��� MgSO4 ��Һ��ֱ������ | |
| D�� | �� Na2SiO3��Һ����ε������ᣬֱ������ |
| A�� | +6 | B�� | +3 | C�� | +2 | D�� | 0 |
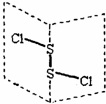 ���Ȼ�����S2Cl2���ǹ㷺������ҵ����������ӽṹ��ͼ��ʾ�������£�S2Cl2��ˮ����ˮ������Ӧ����������ʹƷ����ɫ�����壬����˵���д�����ǣ�������
���Ȼ�����S2Cl2���ǹ㷺������ҵ����������ӽṹ��ͼ��ʾ�������£�S2Cl2��ˮ����ˮ������Ӧ����������ʹƷ����ɫ�����壬����˵���д�����ǣ�������| A�� | S2Cl2�ĽṹʽΪ Cl-S-S-Cl | |
| B�� | S2Cl2��ˮ��Ӧʱֻ��S-Cl���� | |
| C�� | S2Br2���м��Լ��ͷǼ��Լ� | |
| D�� | S2Cl2��H2O��Ӧ�Ļ�ѧ����ʽ����Ϊ��2S2Cl2+2H2O=SO2��+3S��+4HCl |