题目内容
(10分)已知:
(R、R'可表示烃基或官能团)
A可发生如下转化(方框内物质均为有机物,部分无机产物已略去):

请回答:
(1)F的蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1 mol F与足量金属钠作用产生H2 22.4 L(标准状况),则F的分子式是 ,名称是 。
(2)G与F的相对分子质量之差为4,则G具有的性质是 (填字母)。
a.可与银氨溶液反应 b.可与乙酸发生酯化反应
c.可与氢气发生加成反应 d.1 mol G最多可与2 mol新制Cu(OH)2发生反应
(3)D能与NaHCO3溶液发生反应,且两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是 ,
该反应类型是 反应。
(4)H与B互为同分异构体,且所含官能团与B相同,则H的结构简式可能是:
、 。
(5)A转化为B和F的化学方程式是 。
(10分)(1)C2H6O2 (1分) ;乙二醇 (1分)。
(2)a c (1分) 浓H2SO4
(3) CH3-CH-COOH ------→ CH2=CH-COOH + H2O (2分) ; 消去 (1分)
∣ 加热
OH
(4)CH2=CH-CH2COOH (1分);CH3-CH=CH-COOH (1分)
H+
(5) CH3-C-COOCH2CH2OH + H2O -----→ CH3-C-COOH + CH2-CH2 (2分)
‖ 加热 ‖ ∣ ∣
CH2 CH2 OH OH
【解析】略

 阅读快车系列答案
阅读快车系列答案有机物A分子组成为C4H9Br,A中有一个支链,在一定条件下A可发生如下转化:
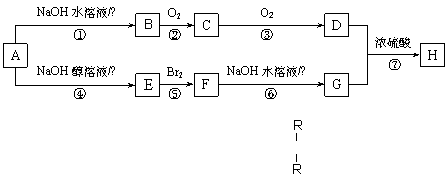 | |||
| |||
已知:连接羟基的碳原子上没有氢原子的醇(如 R—C—OH)不能发生催化氧化反应。
(1)A的结构简式为 ,F的结构简式为 。
(2)上述转化中属于取代反应的有 (填序号)。
(3)反应④的化学方程式为 。C发生银镜反应的化学方程式为 。
E发生加聚反应的化学方程式为 。
(4)反应⑦中,D与G物质的量之比为2∶1,则该反应的化学方程式为:

 ,其中R、R′为烃基。
,其中R、R′为烃基。 , 且属于酯的同分异构体的结构简式 。
, 且属于酯的同分异构体的结构简式 。