题目内容
16.反应2NO+O2=2NO2,不能使该反应的反应速率增大的是( )| A. | 及时分离出NO2气体 | B. | 适当升高温度 | ||
| C. | 增大O2的浓度 | D. | 选择高效催化剂. |
分析 一般增大反应物的浓度、增大压强,升高温度、使用催化剂,化学反应速率加快,以此来解答.
解答 解:A.反应2NO+O2=2NO2,及时分离出NO2气体,生成物的浓度减小,反应速率减小,故A错误;
B.因升高温度,活化分子百分数增大,反应速率加快,故B正确;
C.增加O2浓度,反应物浓度增大,单位体积的活化分子数目增多,反应速率加快,故C正确;
D.选择高效催化剂,加快化学反应速率,故D正确;
故选A.
点评 本题考查影响化学反应速率的因素,题目难度不大,注意常见影响化学反应速率的因素除温度、浓度、压强、催化剂之后还有表面积、溶剂、光照等因素,注意常见基础知识的积累.

练习册系列答案
相关题目
6.将19.5g锌粉加入到2L的0.100mol•L-1 MO2+ 溶液中,恰好完全反应,则还原产物可能是( )
| A. | M | B. | M2+ | C. | M3+ | D. | MO2+ |
11.下列各组中的四种物质,只用一种试剂即可鉴别的是( )
| A. | 淀粉溶液、乙醇、苯、四氯化碳 | B. | 乙烯、乙烷、乙炔、丙烯 | ||
| C. | 甲酸、乙醛、乙醇、乙酸 | D. | 苯酚、溴苯、苯、甲苯 |
1.某同学做如下实验:下列说法正确的是( )
| 装置 | 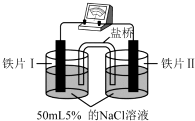 | 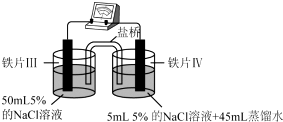 |
| 现象 | 电流计指针未发生偏转 | 电流计指针偏转 |
| A. | “电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 | |
| B. | 用K3[Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极 | |
| C. | 铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,二者的腐蚀速率相等 | |
| D. | 铁片Ⅳ的电极反应式为Fe-3e-=Fe3+ |
2.下列说法正确的是( )
| A. | 某试样焰色反应呈黄色,则试样中含有K+ | |
| B. | 广泛pH试纸测得某碱性溶液的pH为12.5 | |
| C. | 容量瓶不能用作溶解物质的容器 | |
| D. | 粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶 |
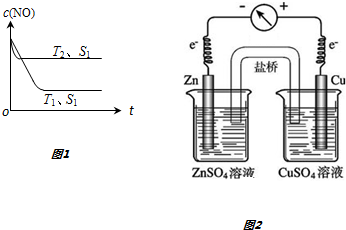
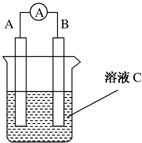 如图所示是原电池的装置图(
如图所示是原电池的装置图( 为电流表).请回答:
为电流表).请回答: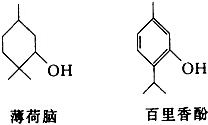 下列物质是几种常见香精的主要成分:
下列物质是几种常见香精的主要成分: .
.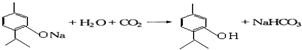 .
.