题目内容
下列反应的离子方程式错误的是
A.NH4HCO3溶液与足量的NaOH溶液混合加热:NH4++HCO3- +2OH- NH3↑+CO32 -+2H2O
NH3↑+CO32 -+2H2O
B.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O
C.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
D.等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合:Ca2++HCO3-+OH-=CaCO3↓+H2O
C
【解析】
试题分析:A、NH4HCO3溶液与足量的NaOH溶液混合加热生成碳酸钠、氨气和水,即NH4++HCO3- +2OH-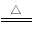 NH3↑+CO32 -+2H2O,A正确;B、Na2SO3溶液具有还原性,使酸性KMnO4溶液褪色,即5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O,B正确;C、碘离子的还原性强于亚铁离子,因此在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸首先氧化碘离子,即6I-+8H++2NO3-=3I2+2NO↑+4H2O,C错误;D、等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合生成碳酸钙、碳酸氢钠和水,即Ca2++HCO3-+OH-=CaCO3↓+H2O,D正确,答案选C。
NH3↑+CO32 -+2H2O,A正确;B、Na2SO3溶液具有还原性,使酸性KMnO4溶液褪色,即5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O,B正确;C、碘离子的还原性强于亚铁离子,因此在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸首先氧化碘离子,即6I-+8H++2NO3-=3I2+2NO↑+4H2O,C错误;D、等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合生成碳酸钙、碳酸氢钠和水,即Ca2++HCO3-+OH-=CaCO3↓+H2O,D正确,答案选C。
考点:考查离子方程式的正误判断

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
 (X为卤素原子)
(X为卤素原子) 的物质,该物质是一种香料。
的物质,该物质是一种香料。
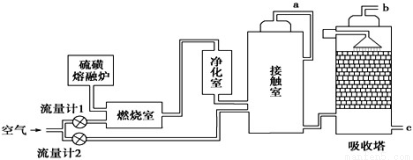
 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是